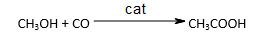En plein hiver et particulièrement dans les régions très froides et montagneuses, il est nécessaire de lutter contre le manque d’adhérence des pneumatiques des véhicules sur sol gelé. On observe alors un ballet de saleuses, qu'on ne doit pas dépasser sur route. Mais que déversent-elles et pourquoi ?
Quels sont les effets du sel ?
.png)
Le sel ou chlorure de sodium de formule chimique NaCl, est soluble dans l’eau liquide. On appelle saumure le mélange liquide eau-sel. L’eau pure devient solide à 0°C sous la pression atmosphérique. Mais si l’eau est salée, ce mélange devient solide à une température inférieure à 0°C.
Ce phénomène est traduit par la courbe de congélation (ci-contre) qui indique la température pour laquelle l’eau devient de la glace, en fonction de la teneur (1) en sel dans le mélange. Comme le montre cette courbe, plus on ajoute de sel, plus la température de congélation baisse. Mais il y a une limite, repérée par le point E, nommé eutectique ! (2) Ainsi inutile de mettre plus de 23 g de sel pour 100 g de mélange, car les cristaux de sel ajoutés restent solides sans pour autant abaisser davantage le point de congélation. Donc ne gaspillons pas !
Et s’il fait une température inférieure à - 21°C, on a beau mettre du sel, la glace ne fond pas (3). Dans la pratique l’ajout de sel n’est plus efficace pour dissoudre la glace en dessous de -10°C, le phénomène de dissolution étant trop lent.
Les salages des routes
Les salages préventifs (la baisse de température est annoncée et imminente) se font pour empêcher l'eau de geler sur la chaussée, pour des températures entre -2° et -8°C.
Les salages curatifs (le verglas ou la neige sont déjà là !) se font avec un mélange de chlorures de sodium, de calcium (CaCl2) ou de magnésium (MgCl2), pour des températures inférieures à -8°C. En effet avec ces sels, les courbes de congélation des mélanges eau/sel de calcium ou magnésium ont des températures eutectiques plus basses (4).
L’épandage par une saumure liquide préalablement préparée, permet une diminution de la quantité de sel utilisée et son effet est beaucoup plus rapide. Il faut des saleuses adaptées.
En Amérique du Nord et au Canada, il est utilisé presque exclusivement du chlorure de calcium, compte tenu des températures hivernales très basses.
Les quantités de sel (NaCl) utilisées sont considérables
Elles varient selon les conditions météorologiques et selon qu’il s’agit d’un traitement préventif ou curatif : la fourchette va de 10 g à 15 g voire 20 g de sel par m². En France les quantités consommées sont de l'ordre 500 000 t à 1 Mt suivant les hivers plus ou moins froids.
Dans les agglomérations françaises, le sel représente l’essentiel des produits fondants utilisés (>99,5%). Environ 51% de la production mondiale de sel est consacrée à l'entretien des routes dans les pays froids. Le sel est actuellement le fondant de verglas le plus économique (environ 80 € la tonne).
Environnement
Ce sel engendre une pollution saline des bords de route, des eaux de surface, mais aussi des nappes phréatiques. Cela a un impact sur les sols, perturbe le système racinaire des plantes, bouscule les écosystèmes aquatiques (rivières et lacs) et favorise la corrosion de certaines infrastructures métalliques.
Différents produits alternatifs (majoritairement des composés organiques) sont recherchés et testés à la fois sur leur efficacité pour la viabilité des routes et sur leur impact environnemental (biodégradabilité, influence sur la demande biochimique en oxygène, …). Il faut aussi que leurs coûts restent compétitifs.
Par exemple, des formiates de sodium, HCOONa ou de potassium, HCOOK, déjà utilisés au Canada et en Finlande, sont très efficaces mais leur biodégradabilité reste un souci et ils sont respectivement 12 et 22 fois plus chers que le sel.
L’Estorob Bio D-Icer est une huile végétale à base de colza, déjà principalement utilisé dans les aéroports. Ce produit est à la fois biosourcé et biodégradable et s'avère 7 fois moins corrosif que le formiate de potassium et l'acétate de potassium. Il n'est pas corrosif vis-à-vis des métaux et freins carbone des avions. Mais il est aussi 11 fois plus cher que le sel (5).
De nombreuses autres études et essais pour des solutions plus écoresponsables sont réalisés de par le monde et la route de « cinquième génération » dotée de multiples fonctionnalités est à venir ! (6)
Françoise Brénon et l'équipe Question du mois
(1) Il s’agit plus précisément de la fraction massique, w, définie par :
w = masse du sel / masse du mélange eau-sel
(2) La lettre E pour Eutectique, qui signifie en grec « qui fond bien ». En effet l’abscisse du point E correspond à la fraction massique eutectique pour laquelle le mélange eau/sel a la température de fusion/congélation la plus basse, appelée température eutectique.
(3) En dessous de -21°C, selon les proportions en sel ajouté, il ne coexiste que des solides : eau solide (glace), NaCl solide ou solides en mélanges hétérogènes.
Dans la pratique on peut déverglacer un sol jusqu’à -30°C avec du chlorure de calcium ou du chlorure de magnésium car leurs températures eutectiques valent respectivement environ -51 °C et -33°C.
(5) On consultera avec intérêt l’étude sur la phytotoxicité de produits alternatifs au sel de déneigement (PDF) réalisée par l’ENSAIA et l’Université de Lorraine.
Voir Les infrastructures des transports : les apports de la chimie dans les projets d’avenir, Henri Van Damme (pages 34 et suivantes).
On entend parler de bon et de mauvais ozone ; cette question a-t-elle un sens ?
Première phrase rencontrée : Le trou de la couche d’ozone nous met en danger, l’ozone est « bon ».
L’ozone dit stratosphérique (*) se forme dans la haute atmosphère sous l’action des rayonnements UV (ultraviolet) très énergétiques provenant du soleil (**). En absorbant des rayonnements UV-C, une petite quantité de dioxygène O2 se transforme en ozone O3. Celui-ci instable, redonne en partie du dioxygène, en absorbant d’autres rayonnements UV-C. Il s’établit naturellement un équilibre dynamique d’équation :
3 O2 = 2 O3
Il se créé ainsi une « couche d’ozone » essentiellement présente entre 20 et 40 km d'altitude et de concentration comprise entre 2 et 8 ppm.
Ainsi, l’ozone stratosphérique est indispensable car il nous protège de rayonnement solaire ultraviolet.
Toute perturbation de cet équilibre faisant diminuer la teneur en ozone en la consommant par des réactions parasites est donc source de danger. La Fondation belge contre le Cancer rappelle que plus la couche d'ozone est mince, moins elle arrête les rayons UV, et plus l’intensité du rayonnement UV est intense à la surface du sol terrestre. C'est au-dessus de la Nouvelle-Zélande et de l'Australie que la couche d'ozone est la plus mince [1]. Les modèles informatiques prédisent qu’une diminution de 10 % de la concentration d’ozone stratosphérique pourrait provoquer chaque année 300 000 cancers cutanés, 4500 mélanomes et entre 1,60 million et 1,75 million de cas de cataracte de plus dans le monde [2]. Sans compter que les UV-B ont aussi des répercussions importantes sur les animaux, les organismes marins et les végétaux.
La mise en évidence en 1974 de la responsabilité des CFC (chlorofluorocarbure) dans la destruction de l’ozone stratosphérique (formation d’un trou au niveau de l’Antarctique au cours du printemps austral) a conduit aux accords de Montréal en 1987, limitant leur utilisation. Les scientifiques prévoient que la couche d’ozone dans l’Antarctique ne retrouvera son niveau initial (d’avant les années 1980) que vers 2050 à 2070, car la durée de vie des CFC est importante [3].
Deuxième phrase rencontrée : La présence d’ozone nous met en danger : l’ozone est « mauvais ».
C’est dans les années 1970 que Paul Crutzen (prix Nobel de chimie en 1995) montra que l’ozone est à la fois produit mais aussi détruit dans la troposphère (basses couches de l’atmosphère (*)) grâce à des réactions photolytiques (action de la lumière, ici UV-B) faisant intervenir des oxydes d’azotes [4].
| D’une part production d’ozone | D’autre part consommation d’ozone |
NO2 → NO + O● | NO + O3 → NO2 + O2 |
Les oxydes d’azote proviennent essentiellement des secteurs de l'industrie et de la production d'énergie (chauffage urbain entre autres) mais aussi des gaz d’échappement des véhicules à essence et diesel malgré l’usage des pots catalytiques qui en limitent le rejet [5].
Des études postérieures montrent que la formation d’ozone est également liée à la présence de Composés Organiques Volatils (COV), dont 10 % sont issus des activités industrielles et urbaines et 90 % sont d’origines naturelles (***) [6].
Ainsi l’ozone troposphérique est un polluant secondaire issu des polluants primaires que sont les NOx et les COV.
Concrètement la formation d’ozone dépend à la fois des quantités d’oxydes d’azote NOx et de COV présents dans la troposphère mais aussi du rapport de la quantité de COV par celle de NOx.
Cette chimie complexe explique que si l’ozone se forme en milieu urbain essentiellement par la présence des oxydes d’azote sa concentration n’y est pas maximale mais qu’elle l’est en milieu rural proche de la ville car la production de COV par la végétation y est plus forte et celle de NOx plus faible [6], [7].
En quoi cette accumulation d’ozone, accentuée depuis l’ère industrielle est-elle néfaste ?
C’est d’abord un gaz à effet de serre qui va donc participer au réchauffement de la troposphère [6].
C’est aussi un puissant agent oxydant pouvant générer des radicaux hydroxyles (HO●) selon les réactions [7]
O3 → O2 + O● suivi de O● + H2O → 2 HO●
Ces radicaux hydroxyles ont une grande importance sur la santé humaine, en provoquant des problèmes respiratoires et des irritations ophtalmiques.
L’ozone intervient aussi dans le dépérissement de la forêt [8] et nos productions alimentaires souffrent de l’augmentation de ce polluant dans la troposphère ; ainsi la production des tomates ou du blé pourraient être diminuée de 10 % dans les zones les plus polluées (Asie et pays méditerranéens) [9].
Ces dernières années des études épidémiologiques suggèrent que l’ozone troposphérique pourrait jouer un rôle dans le développement et la progression de l’insulino-résistance, associée au diabète de type 2 [10].
Du bon usage de l’ozone dans certaines applications industrielles [11].
Dans le cadre d’usage industriel, l’ozone est produit sur le site d’utilisation par décharge électrique à haute tension dans un flux d’oxygène.
L’ozone étant un oxydant puissant il est utilisé dans différentes étapes du traitement de l’eau pour obtenir de l’eau potable mais aussi pour traiter les eaux usées ainsi que de nombreux effluents industriels. Il sert pour la désinfection des eaux de certaines piscines en remplacement de l’eau de javel. Parmi les applications industrielles, on peut citer son usage dans certains procédés de blanchiment de la pâte à papier et dans l’agroalimentaire pour le blanchiment du sucre de canne.
Autres sources d’ozone et cadre professionnel [12].
Quant à la santé au travail, une attention particulière est apportée aux professionnels utilisant des appareils (imprimantes, photocopieuses, spectrophotomètres) utilisant des rayonnements UV ou laser susceptibles de former de l’ozone à partir du dioxygène.
Lydie Amann et l’équipe Question du mois
(*) La troposphère est la partie de l’atmosphère comprise environ entre 0 et 15 km de la Terre. La stratosphère est comprise environ entre 15 km et 50 km de la terre.
(**) Les rayonnements sont caractérisés par leur longueur d’onde exprimée en nanomètres (nm) : UV-B : 280−315 nm ; UV-C : 100−280 nm. Les UV C sont les plus énergétiques.
(***) COV liés à l’activité humaine et industrielle : évaporation d’hydrocarbures lors du raffinage, ou de solvants organiques ou de carburants imbrûlés non retenus par les pots catalytiques ;
COVB ou COV biogéniques, d’origine naturelle : émis par les plantes ou certaines fermentations végétales ou animales. Ils se biodégradent plus ou moins lentement.
Pour en savoir plus :
(1) Rayonnement ultraviolet, site de la Fondation contre le Cancer
(2) Effets du rayonnement UV sur la santé, site de l’Organisation mondiale de la santé
(3) 2019 Ozone Hole is the Smallest on Record Since Its Discovery, site de la NASA (National Aeronautics and Space Administration)
(4) Le prix Nobel 1995 couronne la chimie vitale de la stratosphère, L’Actualité chimique n° 192 (décembre 1995) p. 57
(5) Les oxydes d’azote (NOx) : définition, sources d’émission et impacts, site de l’ADEME (Agence de la transition écologique)
(6) Les défis de la santé et du bien-être en ville : pollution atmosphérique, nuisances thermiques, odeurs, de Jacques Moussafir, in La chimie et les grandes villes (EDP Sciences 2017), pp. 193-216
(7) L'ozone troposphérique : production/consommation et régimes chimiques, de Marie Camredon et Bernard Aumont, Pollution atmosphérique, n° 193 (janvier-mars 2007) pp. 51-60 (voir Figure 2 : Profil type de la vitesse de production d'ozone en fonction de la quantité de NOx)
(8) État des forêts d’altitude en relation avec la pollution de l’air par l’ozone dans la région niçoise, de Laurence Dalstein-Richier et al., Pollution atmosphérique, n° 193 (octobre-décembre 2005) pp. 503-519
(9) Impacts de l’ozone sur l’agriculture et les forêts et estimation des coûts économiques, de Jean-François Castell et Didier Le Thiec, Pollution atmosphérique, n° 229-230 (avril-septembre 2016) pp. 142-152
(10) Pollution atmosphérique et diabète… Quel lien possible ? Une exposition expérimentale à l’ozone chez le rat induit une insulino-résistance périphérique, de Roxane E. Vella, Alain Géloën et Christophe O. Soulage, Pollution atmosphérique, n° 231-232 (octobre-décembre 2016) pp. 105-116
(11) Oxydation et réduction appliquée au traitement de l’eau- Ozone, de Sylvie Baigh et Pierre Bouchet, Techniques de l’ingénieur, mars 2017
(12) Ozone : Fiche toxicologique n° 43, site de l’INRS (Institut national de recherche et de sécurité pour la prévention des accidents du travail et des maladies professionnelles)
Différentes sortes d’agents infectieux provoquent maladies et infections chez l’Homme. Cela peut être des parasites, des champignons, des bactéries, des virus. On a aussi eu le prion, il y a plusieurs années.
Les parasites
Les parasites sont des êtres vivants qui vivent aux dépens d’un autre organisme appelé l’hôte. Par exemple, le sarcopte responsable de la gale, qui est un acarien (Fig. 1), les vers comme le ver solitaire, des protozoaires comme l’agent de la malaria. Ce sont tous des eucaryotes (1) ce qui signifie que leurs cellules ont un noyau, comme les nôtres.
Les champignons et les levures
L’infection provoquée par les champignons et les levures est alors appelée une mycose ou une infection fongique. Champignons et levures sont aussi des organismes pluricellulaires eucaryotes. Ils causent des maladies souvent de la peau (teigne) et des muqueuses (bouche, muqueuses génitales), mais peuvent aussi causer des infections bien plus graves des organes internes comme les poumons (Aspergillus fumigatus par exemple) (Fig. 2).
Les bactéries
Louis Pasteur, Robert Koch sont des pionniers de la bactériologie. Les bactéries (2) ne sont pas des eucaryotes, mais des procaryotes (3), qui n’ont pas de noyau. Ce sont les plus connus des agents infectieux : Escherichia coli, Staphylococcus aureus (staphylocoque doré), Vibrio cholerae (bactérie du choléra), Mycobacterium tuberculosis (tuberculose). Comme les bactéries diffèrent des cellules humaines, les médicaments qui les éliminent sont moins toxiques que les antiparasitaires ou les antifongiques. Mais le problème est la résistance bactérienne : les bactéries devenues résistantes ne sont plus éliminées par les antibactériens et l’infection ne guérit pas. C’est devenu un problème très important.
Parasites, champignons, bactéries sont tous des organismes vivants, capables en général de vivre et de se multiplier dans un milieu nutritif acellulaire : un peu de sucre, de graisse et de protéines (bouillon de culture).
Les virus
Schématiquement, les virus (4) sont des sacs contenant des molécules biologiques, acides nucléiques, protéines ; plus exactement, ce sont des acides nucléiques enfermés dans une capside protéique (Fig. 4 et Fig. 5) ; ils n’ont pas de système métabolique (5). On dit alors qu’ils ne sont pas vivants, en ce sens qu’ils ne peuvent pas vivre et se multiplier dans un bouillon de culture comme le font les agents précédents. Ils ont besoin d’une cellule hôte « qui fait le travail pour eux » : quand ils y entrent, ils lui transmettent leur acide nucléique, ADN (6) ou ARN (7). Pour cultiver les virus, on cultive des cellules, puis on les infecte par le virus. Une fois fixé sur la cellule, le virus va fusionner avec elle. À ce moment, il libère à l’intérieur de la cellule son acide nucléique, et c’est la machinerie enzymatique de la cellule infectée qui se chargera de répliquer ces acides nucléiques et in fine d’aboutir à un ARN messager traduit en protéines pour le compte du virus. On va ainsi synthétiser d’autres virus, qui vont se créer une enveloppe au moyen de celle de l’hôte (Fig. 7), sortir et se disséminer. La cellule hôte est ainsi affaiblie, ce qui conduit le plus souvent à sa mort par lyse (8) : elle éclate, libérant les particules virales qui vont infecter d’autres cellules, etc.
Parmi les virus capables d’infecter l’Homme, il y a ceux qui donnent la grippe ou plutôt les grippes, la poliomyélite, l’hépatite A (jaunisse), la fièvre jaune, la variole, le SIDA, le virus Ebola (fièvre hémorragique), les virus oncogènes - capables d’entraîner des cancers, etc. Ils sont responsables de nombreuses épidémies et même pandémies, souvent respiratoires apparues depuis un siècle, la première étant la grippe espagnole de 1918, qui a causé près de 30 millions de morts. En 1957-1958, la grippe asiatique a entrainé 2 millions de morts ; en 1968-9 la grippe de Hong-Kong, 1 million. Durant les six dernières années, nous avons eu au moins six grandes épidémies.
Et le coronavirus ?
Son nom officiel est coronavirus SARS-CoV-2, en français SRAS pour Syndrome Respiratoire Aigu Sévère. Le nom « Covid-19 « que l’on trouve parfois désigne la maladie et non le virus qui la provoque, 19 indiquant l’apparition en 2019. C’est un coronavirus (9), car l’enveloppe virale (Fig. 4 et Fig. 5) est « décorée » de protéines qui forment des protubérances, dont le cliché en microscopie électronique rappelle les images de la couronne solaire. Ce sont ces protéines qui permettent au virus de se fixer sur la cellule et d’y entrer. Les coronavirus sont des virus à ARN. Ils ont été découverts dans les années 1930 dans des élevages de volailles où ils causent diverses infections. On connaît 7 coronavirus responsables de maladies chez l’Homme, allant d’infections de l’appareil respiratoire bénignes (rhumes et maux de gorge) à graves et à très graves (SARS et MERS).
Ces coronavirus sont d’origine animale, probablement les chauves-souris, puis transmises à des mammifères (civette, dromadaire…) ou à des oiseaux (volailles de marché en Chine). Une fois franchie cette barrière entre espèces, la transmission d’homme à homme devient très facile. Pour le SARS-CoV-2, on compte à ce jour plus de 9.600.000 cas et près de 500.000 morts dans le monde, les pays les plus touchés étant les USA avec 2.400.000 cas et 120.000 morts, puis le Brésil, le Royaume Uni, l’Italie, la France, l’Espagne, respectivement 54.900, 44.500, 34.600, 29.700, 28.300 morts (10).
Nicole Moreau et l'équipe Question du mois
Notes :
(1) Du grec eu, bien et karuon, noyau
(2) Du grec bacterion, qui veut dire bâtonnet
(3) Du grec pro, avant et karuon, noyau
(4) Du latin virus, venin ; mot établi au XVIe siècle par Antoine Paré
(5) Du grec metabolein. Le métabolisme est l’ensemble des réactions de synthèse, génératrices de matériaux (anabolisme), et de dégradation, génératrices d'énergie (catabolisme), qui s'effectuent au sein de la matière vivante à partir des constituants chimiques fournis à l'organisme par l'alimentation et sous l'action de catalyseurs spécifiques.
(6) ADN : acide désoxy-ribonucléique
(7) ARN : acide ribonucléique
(8) Du grec lusis, action de délier, dissoudre.
(9) Il n’est pas le seul coronavirus, mais est l’un des plus gros, mesurant de 50 à 200 nm de diamètre.
(10) la date du 26 juin 2020 (https://gisanddata.maps.arcgis.com )

Figure 1 : Aceria anthocoptes, image obtenue par microscopie électronique à balayage
Source : Wikimedia
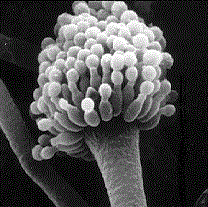
Figure 2 : Aspergillus fumigatus vu au microscope électronique.
Source : Wikimedia
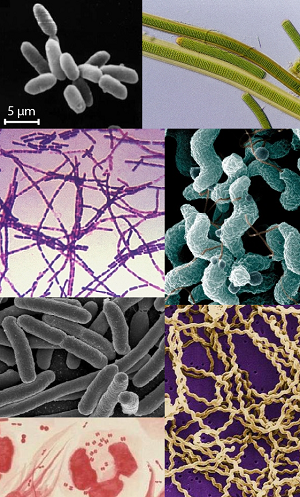
Figure 3 : Différents types de procaryotes
Source : Maulucioni /Wikimedia (licence CC BY-SA 3.0)
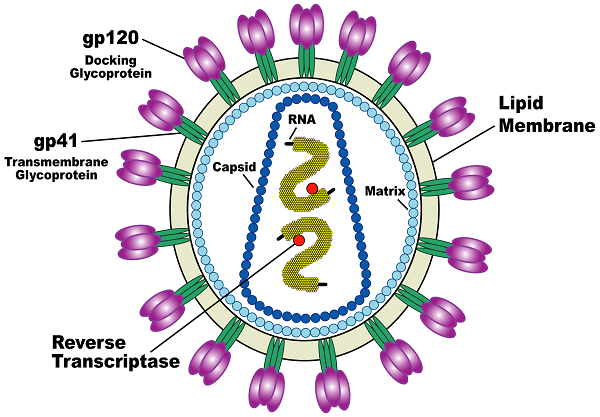
Figure 4 : Représentation schématique d’un virus (HIV)
Source : wikimedia
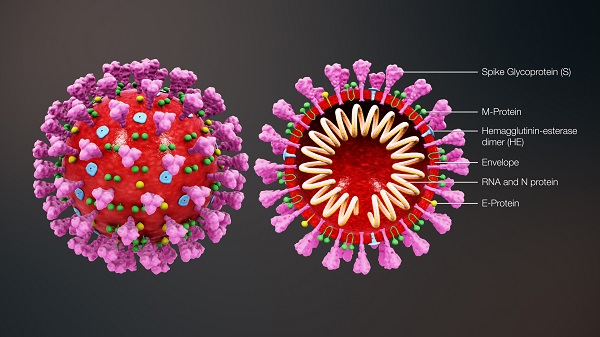
Figure 5 : Représentation schématique d’un coronavirus
Source : https://www.scientificanimations.com (licence BY-SA 4.0)
La radioactivité a été découverte par un français Henri Becquerel en 1896 qui a constaté qu’en enveloppant un minerai d’uranium d’un papier photographique, celui-ci était impressionné en l’absence de toute lumière par un rayonnement inconnu qu’il a baptisé radioactivité.
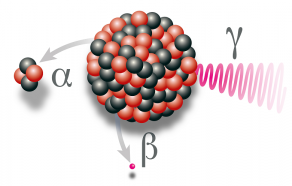
C’est une propriété d’isotopes instables comme l’uranium 238 (238U) ou le thorium 232 (232Th). Marie Curie découvrit plus tard cette même propriété pour le radium (Ra). Les atomes radioactifs comportent dans leur noyau un nombre de nucléons (protons + neutrons) qui rend ce noyau instable. Pour retrouver une configuration stable ils émettent de l’énergie par rayonnement α (noyaux d’hélium, He), β (électrons) ou γ (photons).
La première unité de mesure de la radioactivité fut le becquerel 1 Bq qui correspond à une désintégration par seconde. L’activité d’une source peut s’exprimer en Bq ou en Bq/kg activité massique (1). Notre corps est lui-même radioactif d’environ 120 Bq/kg. Si vous pesez 70 kg, l’activité est d’environ 8 000 Bq due principalement au potassium 40 (40K) et au carbone 14 (14C).
Ce qui est plus important c’est la dose de radioactivité absorbée par une cible, en joules par kilogramme (J/kg). Anciennement appelée rad pour Radiation Absorbed Dose (rad) elle est actuellement, dans le système international (SI) exprimée en gray (Gy) :
1 Gy = 1 J/kg = 100 rad.
Elle trouve son utilité en radioprotection. On définit alors la dose efficace qui est la somme pondérée des doses équivalentes (des rayonnements α, β et γ) absorbées par les organes et tissus humains. Elle est exprimée dans le système international en sievert (Sv) (2) ou son millième, le mSv, unité universellement admise pour la mesure d’exposition à la radioactivité et risques d’apparitions de dégradations de la santé.
Les facteurs de radioactivité
Sur terre nous sommes exposés à plusieurs facteurs. Tout d’abord les rayonnements cosmiques qui nous arrivent du Soleil et de l’espace, le rayonnement tellurique issu des réactions du noyau terrestre et aussi le radon, un gaz lourd radioactif plus ou moins présent dans le sol et le sous-sol, particulièrement dans les régions granitiques. N’oublions pas nos propres activités humaines : si vous passez une radiographie ou un scanner vous êtes exposés aux rayons X (analogues au rayonnement γ), si vous skiez en altitude ou si vous faites des voyages en avion vous serez exposés à plus de rayons cosmiques. Enfin votre propre alimentation vous fait absorber le 40K présent dans les aliments.
| Sources | en mSv par personne et par an |
| Radon | 1,4 |
| Examen médical | 1,6 |
| Rayonnement telleurique | 0,6 |
| Rayonnement cosmique | 0,3 |
| Alimentation | 0,5 |
| Dose moyenne | 4,4 |
Le tableau montre les principales sources et les moyennes, Il peut y avoir de fortes variations suivant les régions habitées, l’altitude fréquentée, l’alimentation absorbée et le comportement individuel.
Quelques exemples et de fausses idées
Pour le radon, dans une cave dans le Cantal, en Lozère ou en Bretagne vous pouvez mesurer des valeurs très variables de 0,5 à 3 mSv. Une radiographie des poumons ou de l’abdomen peut donner des valeurs comprises entre 0,5 et 1,2 mSv, un scanner beaucoup plus. Un voyage aller et retour Paris – New-York, 0,06 mSv, un séjour de ski d’une semaine à 2000 m correspond à 0,25 mSv.
La dose admise réglementairement d’exposition annuelle pour la radioactivité artificielle est de 1 mSv. C’est une norme et ne correspond en rien à une limite dangereuse. Celle-ci est de 100 mSv et correspond à la zone rouge pour la protection des travailleurs du nucléaire pour lesquels on fixe une limite de 20 mSv cumulés sur les 12 derniers mois pour qu’il n’y ait aucune répercussion sur leur formule sanguine.
Les mesures de la radioactivité de l’air se sont multipliées depuis les années 2000, elle est de l’ordre de 100 nSv/h (nSv = nanosievert ou 10-6 mSv). Le réseau de l’IRSN (3) donne pour les grandes villes françaises des valeurs comprises entre 112 et 130 nSv/h. Les retombées radioactives des expériences nucléaires en atmosphère qui ont eu cours jusque dans les années 1970 et l’accident de Tchernobyl en 1986 ne contribuent actuellement à la radioactivité des sols que pour 0,05 mSv, en constante diminution. Les anciens postes de télévision à tube cathodique émettaient des rayons X et pouvaient contribuer à 0,02 mSv par an pour le téléspectateur, les écrans plats n’émettent plus.
D’autres exemples : fumer une cigarette représente 7µSv à cause des goudrons. Combien en fumez-vous ? Si vous mangez beaucoup de crustacés et de coquillages vous absorbez l’iode 131 et le polonium 210 présent dans l’eau de mer mais cela se chiffre en nano et microsievert rassurez-vous. Dans tous les cas le citoyen français en moyenne ne reçoit que de 3 à 4 mSv par an, surtout par radioactivité naturelle, soit une exposition 25 fois plus faible que la dose dangereuse.
Jean-Claude Bernier et l'équipe Question du mois
(1) À côté du becquerel d’autres unités ont été utilisées. Ainsi le curie (Ci) représentant l’activité d’un gramme de radium, soit 1 Ci = 37 109 Bq.
(2) L’ancienne unité pour la dose équivalente et la dose efficace était le rem, pour « röntgen equivalent man ». 1 Sv = 100 rem
(3) IRSN : Institut de Radioprotection et de Sûreté Nucléaire
En 2003 la directive européenne RED (Renewable Energy Directive) a demandé aux pays européens des réductions d’émission de gaz à effet de serre (GES), notamment pour le transport, en faisant appel aux biocarburants capables de diminuer de 35% en 2017 puis de 50% en 2018 les émissions. Les pétroliers ont alors ajouté de l’alcool dans l’essence et des esters d’huiles végétales dans le gasoil, d’origine biosourcée.
Comment fabrique-t-on le bioéthanol (selon les procédés dits de 1re génération) ?
L’éthanol ou alcool éthylique, de formule chimique C2H5OH, est principalement synthétisé lors de la fermentation du sucre, soit de canne à sucre, soit de betterave suivant la réaction :
ou à partir d’amidon de blé ou de maïs, préalablement hydrolysé en sucre, selon :
(C6H10O5)n + n H2O = n C6H12O6 suivi de la fermentation (1).
Lors de ces réactions, l’alcool obtenu est mélangé à de l’eau que l’on doit absolument éliminer.
Pour cela l’opération industrielle se poursuit par une distillation pour obtenir un mélange eau-alcool à 90% (2) en éthanol. Puis les 10% d’eau restants sont éliminés sur tamis moléculaires pour que l’alcool purifié à 99,8% puisse être mélangé à l’essence. Les pétroliers en transforment une partie en ETBE (éthyl ter-butyl éther) (3) par réaction avec l’isobutène (4) afin d’avoir un carburant moins volatil.
Le rendement énergétique de l’éthanol est inférieur à celui de l’essence. En effet le rendement avec un litre et demi d’éthanol équivaut environ à celui d’un litre d’essence. Il faut donc s’attendre pour une automobile à une consommation supérieure au 100 km.
Les différents carburants à la « pompe à essence » : pour quels moteurs ?
En France les différents carburants à essence contiennent des quantités variables d’alcool.
Nom du carburant | SP 95 | SP 98 | SP95 E10 | super éthanol E 85 |
| Logo à la pompe depuis octobre 2018 | E5 | E5 | E10 | E85 |
Pourcentage maximum d’éthanol pur | 5 % | 5% | 10 % | 65 à 85 % selon la saison |
Tous les moteurs modernes sont conçus pour fonctionner avec les 3 premiers carburants.
Par contre pour le E85 il faut une automobile dite « flexfuel » équipée d’un système d’injection et de réglages du moteur lui permettant d’utiliser tous les carburants modulables. Seuls quelques constructeurs commercialisent ces véhicules qui ne représentent à l’achat que 0,3% du neuf. Heureusement depuis 2018 des boitiers électroniques agréés s’adaptent sur les autres automobiles leur permettant de rouler à l’E85 et environ 6000 automobilistes par an y recourent. C’est qu’ils recherchent des économies et une rentabilité car l’E85 est bien moins taxé que l’essence normale (0,12 € au lieu de 0,68 €) ce qui donne un prix moyen de 0,70€/L à la pompe pour l’E85.
Pour une voiture consommant 6 L/100 km de SP 95 à 1,50€/L et équipée pour rouler avec 7L/100 km d’E85 à 0,70 €/L, l’économie est de l’ordre de 4 €. Il faut alors de 20 000 à 25 000 km pour rentabiliser la pose du boitier FlexFuel d’environ 1000€.
[Ajout octobre 2020 : Les données actualisées mensuellement sont disponibles sur le site du Syndicat National des Producteurs d'Alcool Agricole, notamment sur la répartition de l’utilisation des carburants et les coûts et gains d’utilisations du SP95-E10 et du Superéthnol-E85. En 2020, l’estimation d’installations de boitiers est de 3000 par mois.]
Concurrence entre cultures à des fins énergétiques et cultures alimentaires
Alors « sauverons-nous la planète » (5) en roulant au bioéthanol ? La polémique a grossi dès 2010 après des rapports américains qui dénonçaient l’utilisation de cultures vivrières à des fins énergétiques et s’est enflée en 2016 après une étude très documentée de l’ADEME, de l’INRA et d’une ONG « Transport et environnement » pour la Commission de Bruxelles. Non seulement les gains en émission de GES étaient très inférieurs à 30% pour l’éthanol issu des céréales – avec de grandes disparités selon les céréales - mais le chiffrage du CAS (Changement d’affectation des sols) plombait encore ce bilan (6). C’est pourquoi la commission n’a pas voulu augmenter le pourcentage de biocarburants de 1re génération après 2018 comme prévu dans la directive RED.
[Ajout octobre 2020 : Une étude commandée par la Commission européenne a débouché sur la publication en mars 2019 d’un règlement délégué de la Commisssion. Les impacts sur le Changement Indirect d’Affectation des Sols sont détaillés en annexe pour les différentes cultures céréalières, sucrières et oléagineuses. Ces cultures sont classées en dessous du seuil limite de 10% définissant les biocarburants à risque ILUC élevé (risque de changement indirect d’affectation des terres), à l’exception de l’huile de palme dont la valeur est à 45%.]
Quelle est la situation en France ?
Le SP95 E10 est devenu le carburant le plus vendu avec plus de 40% des ventes à la pompe en 2019. L’éthanol représente environ 10% des carburants vendus en France.
Le dernier rapport du ministère de l’Écologie solidaire et celui de la commission parlementaire du 22 janvier précise qu’en 2017 543 millions de litres d’éthanol ont été produits, issus de matières premières française (55% maïs et blé, 33% betterave, 12% divers). De même 753 ML d’ETBE ont été produits à partir de 55% de matières françaises (80% blé et maïs, 18% betterave).
[Ajout octobre 2020 : La production française de bioéthanol utilise moins de 1% de la surface agricole utile nationale.]
Ces deux rapports recommandent d’accélérer la recherche pour l’obtention d’éthanol dit « cellulosique » produit à partir de la biomasse « lignocellulosique » issue de déchets végétaux (bois, paille, bagasses de végétaux), selon des procédés biochimiques.
Pour l’instant des cocktails d’enzymes capables de transformer la cellulose en sucres ont été trouvés et on sait à la fois séparer la lignine et mener la fermentation en bioréacteurs mais le coût de l’alcool produit n’est pas encore compétitif. En France le projet Futurol mené par 11 participants, dont l’IFPEN (8), est arrivé à son terme en 2018 après dix ans de recherche. La bioraffinerie pilote de ce projet à Pomacle-Bazancourt dans la Marne a été cédée à la société ARD (Agro Industrie Recherches et Développements) chargée de son maintien et de la commercialisation de cet éthanol cellulosique français pour le biocarburant 2G (9).
Un peu d’histoire (un retour aux sources ?)
L’inventeur du moteur à explosion, Nicolas Otton, avait conçu ce moteur avec l’alcool comme carburant et le record de vitesse automobile avait été obtenu en 1903 à 177 km/h sur une Gobron-Brillé roulant à l’éthanol. C’est seulement quand les hydrocarbures sont devenus moins chers que l’essence a remplacé l’alcool.
La production de futurs biocarburants respectant les enjeux environnementaux et économiques est un défi exaltant auquel doivent répondre les chimistes et bio-technologistes. Pour nous, automobilistes dans une société économe des ressources, quel que soit le carburant adoptons une conduite cool et écolo !
L’équipe question du mois
(1) Un schéma présentant les étapes de la production de bioéthanol est disponible sur le site SNPAA des Industriels de l'Alcool et du Bioéthanol
(2) Il s’agit de la fraction molaire en éthanol du mélange eau/éthanol
(3) Le nom ETBE est le nom industriel. Son nom selon la nomenclature est le 2-éthoxy,2-méthylpropane.
(4) La réaction mise en jeu entre l’isobutène et l’éthanol pour donner l’ETBE est
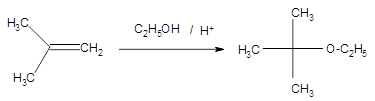
(5) Un exemple d’énergie renouvelable : l’essence verte
(6) Les enjeux de la R&D en chimie pour le domaine des carburants et biocarburants
(7) Polémiques dans le monde des biocarburants
(8) IFPEN : Institut Français du Pétrole et des Énergies Nouvelles
Il est très fréquent d’entendre parler de pile à hydrogène, de voitures à hydrogène, de véhicule « propre », de mobilité hydrogène, de mobilité verte, d’hydrogène vecteur d’énergie, d’hydrogène gris ou vert…
Mais de quel hydrogène parle-t-on ?
Il s’agit de la molécule de dihydrogène, H2, gaz qui n'existe quasiment pas à l'état naturel sur Terre.
En effet, l’élément hydrogène, de symbole H, est très abondant sur la Terre mais seulement sous forme combinée :
- soit avec l’oxygène dans la molécule d’eau, H2O,
- soit avec le carbone dans les hydrocarbures, comme le gaz naturel ou méthane (CH4) ou le pétrole ; ce sont des mélanges de composés de formules générales CnHm
- ou encore dans les molécules du vivant.
Si l’on dispose de dihydrogène, il est possible de récupérer de l’énergie soit sous forme de chaleur via sa combustion directe avec le dioxygène (1) - c’est le cas des moteurs à hydrogène - , soit sous forme d’électricité via une pile à combustible (2) . Dans les deux cas la réaction globale ne produit que de l’eau selon :
2 H2 + O2 →2 H2O
Ainsi le dihydrogène est un vecteur d’énergie mais pas une source d'énergie car n'existant pas à l'état naturel, il faut préalablement le produire à partir d’eau ou d’hydrocarbures, ce qui nécessite d’abord une dépense d’énergie.
L’hydrogène gris ou comment créer du dihydrogène à partir des hydrocarbures
Le réformage (ou reforming) du gaz naturel (3) est actuellement la principale source de dihydrogène. Du méthane et de l’eau sont mis à réagir à haute température (nécessitant donc une consommation d’énergie). La réaction mise en jeu est :
CH4 + H2O = CO + 3H2 suivie de CO + H2O = CO2 + H2
On peut aussi faire le réformage des hydrocarbures liquides (pétrole) ou du charbon (4) .
En plus de la consommation d’hydrocarbures, on notera que pour faire 1 kg d’hydrogène par réformage, on émet de 6 à 10 kg de CO2.
L’hydrogène décarboné ou comment créer du dihydrogène par électrolyse de l’eau
L’apport d’énergie électrique via deux électrodes, plongées dans de l’eau en milieu basique (ou de l’eau acidifiée), reliées aux bornes d’un générateur de courant continu, permet la décomposition de l’eau et la création de dihydrogène, selon la réaction :
2 H2O → 2 H2 + O2
Dans quel cas cet hydrogène décarboné est-il « vert » ?
Tout dépend de la source d’électricité. Si elle provient d’une centrale à charbon, d’une centrale à fuel lourd ou au gaz, cet hydrogène reste gris ! Si la source d’électricité est elle-même décarbonée et renouvelable, courant électrique provenant de barrages hydrauliques, d’éoliennes ou de panneaux solaires, on parle d’hydrogène vert.
Le grand intérêt de cette électrolyse est de permettre le stockage de l’énergie sous forme de dihydrogène pour ces sources intermittentes d’énergie avant de récupérer ultérieurement l’énergie via sa combustion dans une pile à combustible ou dans un moteur. C’est en ce sens que l’hydrogène vert participera à la transition énergétique.
Toutefois il faut garder à l’esprit que chacun des rendements de l’électrolyse et de la pile à hydrogène sont inférieurs à 1 et que le stockage consomme aussi de l’énergie (5) .
Françoise Brénon et l'équipe Question du mois
(1) La combustion du dihydrogène
Sa combustion en présence d’oxygène génère de l’eau selon 2 H2 + O2 →2 H2O, et s’accompagne d’un très important dégagement de chaleur (143 kJ pour un gramme de H2 soit trois fois plus que l’essence ou le diesel).
Comme c’est un gaz très léger, 11 fois plus léger que l’air, il faut pour l’utiliser, le comprimer très fort ou le liquéfier. C'est ainsi l'un des combustibles liquides les plus utilisés au décollage, dans les étages cryogéniques des lanceurs de fusée. Par exemple, la navette spatiale Ariane 5 emporte jusqu'à 26 tonnes d'hydrogène liquide dans ses réservoirs !
Schématiquement, la pile présente deux compartiments alimentés par du dihydrogène à l’anode et de l’air à la cathode. Quand la pile débite, la réaction globale est la même réaction que celle de la combustion directe, soit
2 H2 + O2 → 2 H2O. Voir https://www.mediachimie.org/sites/default/files/FR-pile-images.pdf
Ainsi des voitures électriques, munies d’un réservoir à dihydrogène comprimé, peuvent fonctionner avec le courant continu délivré par une pile à hydrogène, le dioxygène provenant en continu de l’air. Ces voitures, lors de leur fonctionnement, émettent seulement de la vapeur d’eau et non plus des oxydes d’azote ni de dioxyde de carbone. C’est ainsi que l’on parle de « véhicule propre ».
(3) Le réformage du méthane nécessite de travailler entre 800 et 900 °C et sous 350 bars, en présence de catalyseur à base d’oxyde de nickel sur des anneaux d’alumine imprégnés par 10 à 16 % en masse de Ni (leur durée de vie est comprise entre 8 et 10 ans).
(4) Les matières premières utilisées, dans le monde, pour produire le dihydrogène, en 2014 sont à 96 % d’origine fossile.
gaz naturel | hydrocarbures liquides | charbon | électrolyse |
49% | 29% | 18% | 4% |
(5) Globalement l’électrolyse de l’eau, le transport et la compression du gaz à 700 bars consomment environ 75 % de l’énergie que l’on aurait pu récupérer lors du fonctionnement de la pile. En effet, pour qu’un véhicule fonctionne avec une pile à hydrogène vert, il a été nécessaire en amont de faire l’électrolyse de l’eau, d’acheminer le dihydrogène à la station et enfin de comprimer fortement le gaz pour qu’il occupe un volume réduit dans la voiture. On admet que l'électrolyse de l'eau a un rendement compris entre 50 et 60 % par rapport à la puissance électrique fournie. Les rendements de l’électrolyse à haute température peuvent monter plus haut (80 à 90 %) mais il faut faire de la vapeur à 300-800 °C. Enfin il faut comprimer le gaz à 700 bars (de l’énergie est donc dépensée par le compresseur) et la température du gaz s’élève (selon la loi pV=nRT), gaz qu’il faudra refroidir après.
Les piles alcalines, les piles boutons, les batteries ont envahi notre vie de tous les jours. Elles apportent l’énergie électrique aux jouets, aux lampes torches, aux téléphones et tablettes portables, aux véhicules automobiles… Notons bien en français la distinction « pile » chargée une fois pour toute et qui se décharge à l’utilisation et « batterie » ou accumulateur qui délivre un courant grâce à une réaction électrochimique réversible et qui peut se recharger.
90 % des piles sont des piles « alcalines ». On trouve les « piles bâtons » cylindriques qui ont une anode constituée de zinc métallique (Zn) en poudre et d’un électrolyte gélifié contenant de l’hydroxyde de potassium (KOH). La cathode est constituée d’un mélange de dioxyde de manganèse (MnO2) et de carbone graphite (C) le tout enserré dans un cylindre d’acier.
Les piles boutons comportent souvent un gel de zinc et de potasse (KOH) et de l’argent (Ag), puisque le mercure (Hg) est maintenant interdit.
Les batteries rechargeables sont diverses :
- batteries nickel-cadmium (1), Ni-Cd, pour les outils de bricolage autonomes ;
- batteries nickel-hydrures métalliques de terres rares et de nickel (2), Ni–MH, pour les ordinateurs et les téléphones ;
- et de plus en plus de batteries Li-ion (3) (ion lithium) qui comportent une anode en graphite et des cathodes avec des oxydes mixtes de cobalt de type LiCoO2 , ou nickel, ou manganèse.
Sachant que l’on utilise environ 33 000 tonnes de piles et batteries en usage par an, cela représente environ 10 000 tonnes de zinc et 8 000 tonnes de fer et nickel sans oublier le cuivre.
Il ne faut donc surtout pas les jeter dans la nature ou dans les poubelles car vous dispersez alors partout des métaux lourds comme Zn, Fe, Co, Mn, et pire, des métaux pouvant être toxiques comme Ni ou Cd ainsi que des métaux rares et coûteux comme Cu, Ag et des terres rares : néodyme (Nd), praséodyme (Pr), dysprosium (Dy) et lanthane (La).
Une attitude d’éco-citoyen responsable exige aussi une économie des ressources naturelles et c’est une raison de plus pour mettre piles et batteries dans les bacs spécialisés de recyclage que l’on rencontre dans toutes les grandes enseignes de supermarchés ou de bricolage.
| Sur 100 piles utilisées | ||
| 30 sont jetées aux ordures ou dans la nature | 35 sont stockées ou en usage chez les particuliers | 35 sont recyclées par les filières existantes |
L’objectif est de développer les procédés de recyclage par broyage, puis hydrométallurgie et pyrométallurgie pour récupérer les alliages ferreux et affiner les métaux non ferreux ou rares.
Les directives européennes de recyclage sont d’en atteindre au moins 45 % par des organismes nationaux agréés, comme Corepile ou Sorelec, qui, en France, se partagent le recyclage d’un peu plus de 12000 tonnes de piles et batteries.
Dans le cas particulier de l’industrie automobile, où la plupart des véhicules sont équipés de batteries au plomb et acide sulfurique, il y a obligation de les recycler. Plus de 95 % sont désossées, l’acide est neutralisé, le plomb refondu et le polypropylène des caissons lavé et transformé en granulés recyclables.
Avec l’augmentation des véhicules électriques et des millions de tonnes de batteries ion–lithium qui s’annoncent, des filières spécialisées vont se mettre en place pour récupérer et recycler Cu, Co, Ni, Mn et Li.
Donc quand vos piles ou batteries ne fonctionnent plus, ne les jetez plus n’importe où et pensez recyclage, les chimistes s’en occupent pour une seconde vie (4).
Jean-Claude Bernier et l'équipe Question du mois de Mediachimie
(1) Une des électrodes est en oxyde de nickel hydraté NiO(OH) et l’autre est en cadmium, Cd.
(2) Une des électrodes est composée d’un hydrure métallique à base de lanthane (terre rare) et de nickel, de type LaNi5 et l’autre de l'oxyhydroxyde de nickel, NiO(OH). L’électrolyte est de la potasse.
(3) L’Académie suédoise vient de couronner en 2019 les inventeurs des batteries ion-lithium par le prix Nobel de chimie. Pour en savoir plus voir l'éditorial Un Nobel de chimie populaire
(4) Pour en savoir plus, voir la vidéo de l'ADEME ressource Comment transformer nos déchets électroniques en or et autres métaux précieux
Un clin d'œil à la chimie du réveil et du coucher
Quand le soleil se lève…
La couleur bleue du matin éveille en nous la synthèse de multiples molécules chimiques et en particulier au niveau du cerveau de nombreuses molécules dites neuromédiateurs ou neurotransmetteurs. Il s’agit de petites molécules, lesquelles, une fois synthétisées dans les cellules, sont déversées dans le liquide intercellulaire (entre les cellules) pour transmettre des messages relatifs à l’éveil et au tonus (1).
Nos humeurs, notre équilibre affectif, notre appétit, nos motivations durant la journée en dépendent fortement. La sérotonine, la dopamine comme la noradrénaline en font partie (2). Un défaut en sérotonine ou en dopamine peut conduire à des pathologies graves comme, réciproquement, la dépression ou la maladie de Parkinson.
Les sources d’alimentation influencent aussi et pour beaucoup l’approvisionnement de l’organisme en ces deux neuromédiateurs : leur biosynthèse a lieu dans l’organisme à partir des acides aminés dits essentiels c’est-à-dire apportés par la nourriture. Il s’agit du tryptophane pour la sérotonine et de la phénylalanine pour la dopamine (3). Les protéines contenant le plus ces acides aminés sont celles issus du soja, des haricots secs, des lentilles, des graines de noix, œufs, légumes, fruits, poissons et viandes. Dans l’ensemble il faut privilégier plutôt les légumes secs, les lentilles, les noix et non une alimentation hyper-protéinée.
Quand le soleil se couche…
Le soleil tombant, la couleur rougeâtre va changer les processus physiologiques.
Ainsi et à titre d’exemple la synthèse de la sérotonine va être revue à la baisse et le surplus circulant va être transformé en mélatonine (melanas en grec=encre noire), l’hormone qui va progressivement nous conduire vers les bras de Morphée (4).
La lumière, le soleil et le crépuscule remplaceraient abondamment et qualitativement nos réveils électroniques grâce à la chimie et ses impulsions par le simple déclenchement des régulations naturelles. À quand les chambres à coucher rougeâtres la nuit tombante et bleues le soleil levant ?
La preuve de concept étant presque faite, allons plus loin et imaginons des peintures intelligentes dont «l’Homme » aurait grand besoin ! Ses humeurs, son énergie, ses dépressions, son efficacité, sa prductivité au travail et son bien-être ne pourraient que s’améliorer !!
Constantin Agouridas et l'équipe Question du mois de Mediachimie
[1] L’influx nerveux (message) est ainsi transmis à partir des cellules nerveuses (neurones) vers d’autres neurones ou vers d’autres cellules de l’organisme comme les muscles…
[2] Ces trois molécules sont des amines. Leurs formules sont :
| sérotonine | dopamine | noradrénaline, isomère L (R) est seul concerné |
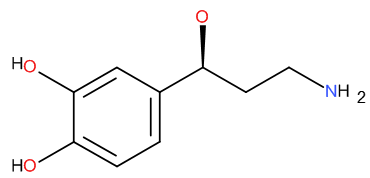 |
[3] La dopamine peut dans certaines circonstances trouver un autre précurseur endogène pour sa biosynthèse : la tyrosine. Il faut noter que la source de la tyrosine dépend aussi de la phénylalanine…
Pour ces 3 acides aminés, seuls les isomères L (S) sont impliqués.
| L (S) phénylalanine | L (S) tryptophane | L (S) tyrosine |
[4]La mélatonine ou « hormone du sommeil » a pour formule
La sérotonine subit une acétylation de sa fonction amine et une méthylation de sa fonction phénol, par voie enzymatique, dans la glande pinéale ou épiphyse, selon :
Bien que la morphine, tire son nom de Morphée, cette molécule complexe, utilisée contre les douleurs intenses, n’est pas synthétisée au sein de l’organisme, mais extraite de l’opium. Elle n’appartient pas au cycle circadien.