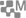Incohérent, irréaliste, niveau indigne d’une production des services de l’État… On n’avait pas l’habitude de voir une publication du ministère de l’Économie, de l’Industrie et de l’Énergie descendue en flammes par les spécialistes de l’énergie de l’Académie des sciences (1). De quoi s’agit-il ? Tout simplement du projet de décret que le gouvernement doit adopter concernant « la programmation pluriannuelle de l’énergie » (PPE3) qui doit engager la France pour les 10 prochaines années jusqu’en 2035 et entrainer des investissements de plusieurs centaines de milliards d’euros.
Que lui reprochent les académiciens ?
Tout d’abord la non prise en compte des remarques et corrections que l’Académie avait soumises en décembre 2024, qui relevait déjà un manque de cohérence sur les valeurs de consommation visées en 2035 : 429, 500 ou 600TWh, laquelle prendre parmi ces divers chiffres ? Des objectifs de production irréalistes et excessifs, en contradiction avec les prévisions qui s’observent non seulement en France, mais dans tous les pays européens avec des besoins qui diminuent depuis 2017.
Si l’Académie soutient une production nucléaire substantielle (300 à 400 TWh) d’énergie bas-carbone à la fois massive et pilotable, elle juge inquiétante voire irresponsable l’augmentation inconsidérée des énergies solaires et éoliennes intermittentes largement multipliées par 3 entre 2023 et 2035 (73 TWh à 270 TWh). Elle souligne de ce fait un excédent d’offre de plus de 100 TWh avec un taux d’électricité non pilotable excessif proche de 40% qui exigerait des capacités de stockage non disponibles y compris en 2035, une priorité sur le réseau de distribution qui entrainera une volatilité des prix considérable avec de périodes de prix très élevés puis négatifs, mortelles pour les couts d’acheminement et de conduite de l’électronucléaire.
Le comité de l’Académie en profite pour rappeler l’avis du Haut-Commissaire à l’Énergie Atomique et du Haut Conseil pour le Climat regrettant aussi que le texte de la PPE ne soit pas accompagné d’une analyse approfondie des coûts et financements des solutions et des divers scénarios recommandés ou alternatifs.
Marc Fontecave, président du comité de prospective en énergie de l’Académie, en profite pour rappeler que la France avec seulement 29% d’énergie intermittente est recordman des exportations (89 TWh), avec un mix électrique qui n’émet que 21,3 g de CO2eq/KWh. À comparer à nos voisins allemands qui avec une part de production solaire et éolienne de 45% affiche une émission de 350 g CO2eq/KWh soit 17 fois plus !
En dehors de la réécriture du texte soumis, l’académie recommande :
- une mise en cohérence des évolutions de la consommation d’énergie
- des capacités pilotables en adéquation avec la puissance appelée
- le renforcement des réseaux électriques
- un effort de recherche technologique sur des moyens de stockage important et peu couteux
- enfin une approche plus réfléchie de la balance production énergie décarbonée et besoins d’électrification.
À titre personnel, je suis sidéré qu’un document de type décret contienne tant d’incohérences et montre aussi peu de réflexions sur les moyens de production énergétique. Sur le site du Ministère de la transition écologique on note que la PPE a fait l’objet d’une consultation nationale avec des dizaines de milliers d’internautes et plus de 7000 contributions ! On ne peut alors que regretter que les contributions de conseils nationaux, de grands experts et de scientifiques spécialistes de l’énergie ne s’y retrouvent pas. J’imagine donc que les 7000 contributions venaient de particuliers peu au courant de la question ou de militants d’une idéologie particulière. C’est un peu comme si on demandait aux jeunes élèves de CP à se prononcer sur la programmation de l’enseignement secondaire. Je n’oublie pas que dans un sondage de 2023 une bonne majorité de Français pensaient que l’électronucléaire émettait énormément de CO2 ! Je pense cependant que les rédacteurs du ministère avaient connaissance des tableaux d’intensité carbone de l’ADEME et du GIEC. Je leur rappelle le tableau ci-dessous qui montre l’inanité de remplacer le nucléaire par l’éolien et le solaire (surtout majoritairement avec des panneaux chinois) qui ont une intensité carbone 2 à 10 fois plus élevée !
J’apprécie qu’une trentaine de scientifiques, et non des moindres, certains ou certaines ayant ou ayant eu des responsabilités considérables, aient souligné la pauvreté sinon les erreurs d’un projet de décret engageant la politique énergétique de la France pour les 10 prochaines années. Il convenait de sonner la charge contre les zozos des cabinets ministériels qui conduisent depuis plus de 20 ans une politique énergétique de gribouille.
Tableau de l’intensité Carbone des différentes sources énergétiques en grammes de CO2eq/KWh
| source | nucléaire | hydroélectrique | éolien | solaire | fioul | charbon |
| GIEC | 5 | 11 | 13 | 30 | 900 | 980 |
| ADEME | 4 | 6 | 15 | 43 (chinois) | 980 | 1080 |
Jean-Claude Bernier
avril 2025
(1) Académie des sciences : avis de l’Académie des sciences sur la version révisée de la programmation pluriannuelle de l’énergie (PPE3) 8 avril 2025
Crédit illustration : David Monniaux, Barrage de Monteynard (Isère, France), Wikimedia commons, licence CC BY-SA 2.5
Il y a quelques années, de nombreuses critiques relatives aux déplacements en avion avaient même appelé au boycott des déplacements aériens. Ces critiques n’étaient pas dénuées de fondement puisque par passager et par kilomètre en avion l’émission était de 140 g de CO2 à comparer aux 3,2 g par TGV. Cela avait amené des États à souhaiter supprimer un certain nombre de vols domestiques lorsque la liaison par rail était tout aussi rapide. Face à ces mesures, paradoxalement, les experts de l’aéronautique prévoyaient au contraire une augmentation du trafic mondial confirmé lors de l’après-COVID avec des chiffres sans appel de 8 milliards de passagers attendus en 2040 contre 4,4 milliards en 2019, et l’arrivée de 40 000 avions neufs dont plus de 18 000 pour remplacer les appareils en fin de vie.
Au niveau mondial, le secteur aérien contribue à quelque 3% des émissions de CO2 (1). Dans un élan louable avant 2020, les 193 États de l’Organisation de l’Aviation Civile Internationale (OACI), se donnaient comme objectif 0% d’émission en 2050. En 2023, cette même organisation était d’accord pour réduire de 5% les émissions d’ici 2030, en recourant au remplacement du kérosène issu du pétrole par des carburants durables appelés SAF (pour Sustainable Aviation Fuels). Pour sa part, dans la foulée, la Commission européenne dans sa directive « ReFuelEU Aviation » souhaitait que les compagnies de transport aérien incorporent des quantités croissantes de SAF dans le kérosène, 2% en 2024 et 6% en 2030. Bémol en 2025 : l’A4E, association regroupant les principales compagnies aériennes européennes, a tenu le 27 mars à Bruxelles une conférence de presse pour contester ces objectifs européens d’incorporation et dénoncer le calendrier irréaliste compte tenu des faibles quantités de SAF disponibles et de leur prix 3 à 4 fois plus cher que le kérosène. Est-ce un nouveau coup de boutoir contre les règles environnementales européennes face à la concurrence internationale ? Essayons d’y voir clair et quelles sont les pistes d’économie ?
Le poids
Faire voler un plus lourd que l’air ce n’est pas facile, il faut de l’énergie pour le faire décoller et voler sur de longs parcours. Quelques dizaines de kilogrammes en moins permettent d’économiser des litres de carburant. Le remplacement progressif de l’aluminium et des métaux (2) par les matériaux composites en polyesters et fibres de carbone comme dans l’A350 d’Airbus où ces matériaux représentent plus de 50% du poids permet d’économiser environ 20% de la consommation (3). Le remplacement du métal des structures des 156 sièges par un alliage de magnésium sur un A319 permet de gagner plus de 500 kilogrammes. EasyJet a fait repeindre une partie de sa flotte avec une peinture ultra légère ne nécessitant plus de nombreuses couches et permettant l’économie de 1300 tonnes de carburant. Cette même compagnie EasyJet a aussi une politique tarifaire pour les bagages et qui consiste à faire payer plus au-delà d’un certain poids et taille. « Voyager léger », c’est le slogan.
Plus sérieux, la fabrication additive des pièces complexes en composite et le remplacement des polymères thermodurcissables par des thermoplastiques recyclables et surtout permettant de souder ces pièces en évitant l’usage de rivets en métal est un progrès. Le couplage de ces nouvelles méthodes de fabrication permettrait encore une réduction supplémentaire de 6% de la consommation.
Les moteurs
On est assez loin pour l’aviation civile du moteur à pistons et à hélice. L’essentiel des flottes long courrier est équipée de turboréacteurs dont les dimensions ont progressé avec leur puissance. Le leader de la construction de ces moteurs est un franco-américain GE Aviation/Safran qui équipe la plupart des nouveaux avions de ligne Airbus et Boeing (4). Ces moteurs comprennent une soufflante qui comprime l’air à l’avant d’une turbine de combustion avec des pales tournant à très haute température (1200°C) en alliages spéciaux et bientôt en CMC (composites céramiques). Les moteurs CFM 56 des Boeing 747 ont été remplacés par les moteurs LEAP pour l’A320 et Boeing737 permettant d’économiser 25% de carburant. Le dernier, le CFM Rise qui sera opérationnel en 2030, comporte déjà de nombreuses pièces fabriquées en 3D, des pales de soufflantes en composites carbone et des aubes de turbines en céramiques composites. Il sera révolutionnaire dans la mesure où les pales de la soufflante ne seront plus carénées et apparaîtront comme des hélices en avant du turboréacteur. Il devrait permettre un meilleur rendement capable d’économiser encore 20% de plus.
Si sur un gros 747, on estimait par passager la consommation à 3 L/100 km sur un A320 à environ 2,8 L/100 km et sur un A350 à 2,5 L/100 km dans les futurs avions avec le nouveau moteur CFM Rise on devrait être aux environs de 2 L/100 km dépendant bien sûr de la taille de l’avion et du nombre de passagers. Safran Electrical & Power vient en février d’obtenir la certification par l’EASA de son moteur électrique ENGINeUS 100 qui est un concentré d’innovation avec l’électronique de puissance qui contrôle son fonctionnement. Autre atout, sa compacité : il affiche une puissance de 125 kW avec un rapport poids puissance de 5 kW/kg. Il est produit à Niort (79) et au Royaume-Uni à un rythme qui sera de 1000 unités par an et s’adapte bien à l’aviation légère 100% électrique pour 1 à 3 passagers, aux avions hybrides pour 19 passagers, etc. (5) Déjà plus de huit compagnies ont passé commande.
Les carburants alternatifs
Les carburants d’aviation durable (Sustainable Aviation Fuel, SAF) neutres en carbone, peuvent être produits suivant 4 grands procédés chimiques (6) :
- les procédés oléochimiques de transformation des huiles végétales, animales, usagées ou non, par hydrogénation (HEFA)
- les procédés biochimiques transformant le sucre en éthanol (ATJ)
- les procédés thermochimiques par gazéification des déchets organiques et Fischer-Tropsch (FT)
- les procédés synthétiques à partir de CO2 et hydrogène (Fischer-Tropsch ou méthanol)
Dans tous les cas les SAF doivent être certifiés par les organismes internationaux de normalisation ASTM pour une utilisation sûre dans le domaine aérien et par l’OACI.
Pour l’instant, en 2025 en France, la voie Fischer-Tropsch est étudiée par Elyse Energy à partir de déchets lignocellulosiques du bois et hydrogénation, la voie ATJ à partir du sucre et de cellulose par Futurol et Global Energy permet d’obtenir un SAF qui a été testé en mars par Safran Aircraft. Seul le procédé HEFA est arrivé au stade industriel notamment en Europe par les sociétés Neste et TotalEnergies. Avant que la bioraffinerie de Grand-Puits soit mise en service en 2025, TotalEnergies jongle sur plusieurs sites, avec la raffinerie de La Mède (13) où arrivent les graisses animales et huiles usagées. Elles y sont prétraitées puis hydrogénées grâce à l’hydrogène venant de l’unité de reformage voisine, puis passent dans l’unité d’isomérisation. Pour séparer le carburant pour l’aviation, il manque un étage de distillation à la Mède, donc le HVO part en Normandie à Oudalle (76) pour obtenir le SAF propre qui est ensuite envoyé à Bordeaux (33), d’où partent les citernes alimentant les aéroports. Ce SAF n'est pas encore complétement neutre en carbone car il y a encore 25% d’huiles végétales de colza et l’hydrogène n’est pas « vert » ! Justement l’hydrogène, me direz-vous ? (7) Pour l’instant le kilogramme d’hydrogène vert vaut à peu près 12 fois le prix du litre de kérosène et Airbus vient d’annoncer qu’il retarde la mise au point de son avion à l’hydrogène ZEROe, devant l’incertitude des infrastructures d’alimentation de ce carburant aux aéroports, c’est montrer que la propulsion aérienne à l’hydrogène n’est pas encore mûre.
Conclusion
Les compagnies aériennes ont raison de dire que les objectifs de réduction des émissions ne seront pas tenus en 2050. Au-delà des annonces et des vols de démonstration, plus médiatiques qu’efficaces, les obstacles sont multiples. Même avec un taux d’incorporation des SAF de 6% en 2030, la production sera largement insuffisante, le procédé d’hydrogénation toujours nécessaire n’est pour l’instant pas nourri d’hydrogène issu de l’électrolyse de l’eau et d’électricité durable. Malgré les efforts d’Airbus et de Boeing, les nouveaux appareils sont livrés au compte-gouttes, empêchant les compagnies d’utiliser les dernières innovations économes en carburant et laissant vieillir leurs flottes. Contrairement à d’autres secteurs de la transition énergétique, l’aviation ne bénéficie pas de subventions mais au contraire de nouvelles taxes frappent le transport aérien.
Devant les doutes sur les ressources et la collecte des millions de tonnes de déchets lipidiques et de biomasse, les investissements dans les filières de HVO (Hydrotreated Vegetable Oil) hésitent et l’engagement d’achat des compagnies aériennes manque. Devant ce cercle vicieux, des experts thermodynamiciens soulignent de plus que la collecte, le prétraitement, l’électrolyse de l’eau, la demande d’énergie pour le raffinage, sont loin d’être négligeables et qu’il conviendrait de faire le bilan carbone de ces SAF. Alors que faire ? Avant de prendre l’avion, faites donc un régime pour maigrir, prenez un petit baluchon très léger, assurez-vous de l’âge récent de l’appareil, sinon prenez le TGV, bien sûr pour New-York ça prendra du temps !
Jean-Claude Bernier
Avril 2025
Pour en savoir plus
(1) Hydrogène, optimisation énergétique et sobriété : l’avenir de l’aviation, P. Labarbe, Fiche Chimie et… en fiches lycées (Mediachimie.org)
(2) Dernières avancées dans les alliages d’aluminium pour applications aéronautiques, T. Warner, colloque Chimie, aéronautique et espace, Fondation de la Maison de la Chimie (novembre 2017)
(3) Les nouveaux matériaux composites pour l’aéronautique, V. Aerts, colloque Chimie, aéronautique et espace, Fondation de la Maison de la Chimie (novembre 2017)
(4) La combustion et les défis de la propulsion aéronautique et spatiale, S. Candel, Colloque Chimie et transports, Fondation de la Maison de la Chimie (avril 2013)
(5) La chimie s’envoie en l’air, J.-C. Bernier, L’Actualité chimique n° 424 (décembre 2017)
(6) La chimie, une solution pour l’avion de demain ?, A. Charles, N. Baffier et J.-C. Bernier, fiche Chimie et… en fiches cycle 4 (Mediachimie.org)
(7) Allons-nous voler à l’hydrogène ? L’évolution du transport aérien, J.-C. Bernier et F. Brénon, éditorial juillet 2021 (Mediachimie.org)
Crédit illustration : Niklas Jeromin / Pexels, libre d'utilisation
L’impression 3D encore appelée couramment Fabrication Additive (FA) a quitté le domaine du prototypage dans les années 1980 pour gagner le domaine industriel et même le domaine ludique après les années 2000. Elle consiste à réaliser des pièces en 3 dimensions par ajouts successifs de couches de matières principalement des polymères ou des métaux. Elle s’oppose donc à la fabrication soustractive dont le principe est de retirer de la matière à une pièce préalablement moulée (1).
Elle présente de multiples avantages : elle repousse les limites de la technologie en réalisant des formes complexes jusqu’ici irréalisables par moulage ou forgeage, elle permet d’optimiser la quantité de matière première et donc de réduire les coûts et elle permet aussi de réduire les déchets.
Quels sont les procédés de Fabrications Additives ?
Le principe repose sur celui des imprimantes à jet d’encre que l’on retrouve dans tous les bureaux, sauf qu’ici on ne projette plus d’encre chargée en noir de carbone mais un polymère fondu ou une poudre métallique. De même, la buse de projection ne se promène plus de droite à gauche au-dessus du papier (2D), mais elle est animée d’un mouvement vertical au-dessus d’un plateau qui bouge horizontalement (3D).
- FDM (Fused Deposition Modelling) est le procédé le plus connu. L’imprimante est alimentée par un filament de moins d’un millimètre de diamètre d’un thermoplastique qui passe dans une buse chauffée à environ 150° à 250°C. Commandés par un logiciel qui contient les données géométriques de l’objet à fabriquer, les mouvements du plateau et de la buse construisent l’objet couche après couche. Des bobines de fils de PLA (acide polylactique) biodégradable, d’ABS (acrylonitrile butadiène styrène) ou de PET (polyéthylène téréphtalate basse et haute densité) sont maintenant disponibles très couramment chez les industriels des polymères et en 2009 l’expiration des brevets FDM popularise cette technique et lui donne un fort développement.
- Autres types de procédés dérivés du FDM :
- FTI (Film Transfer Imaging) utilise un photopolymère ; après dépôt on illumine avec des lampes infrarouges ou un laser UV pour durcir les couches de résine (SLA StéreoLithography Apparatus) ;
- MJM (Modelage à Jets Multiples) dispose de plusieurs buses et des arrivées de mélanges pour avoir des couches de polypropylène et d’acrylates ;
- SLS (Selective Laser Sintering) quitte le domaine des polymères pour la métallurgie. Des couches successives de poudres de métal (aluminium, acier, titane…) sont déposées et sont frittées par un laser IR de puissance (2). Avec les brevets sur le SLS qui ont expiré en 2014, nombre d’entreprises se sont lancées avec des ateliers entiers d’imprimantes à la fabrication de pièces complexes en petites séries pour l’automobile, l’aéronautique et le spatial.
- Autres types dérivés du SLS :
- le SLM (Selective Laser Melting) : on fait fondre à haute température le fil métallique et on dépose des couches de métal fondu.
- le WAAM (Wire Arc Additive Manufacturing) est un peu une déviation de la soudure à l’arc, puisque le fil est une électrode mise en fusion par arc électrique et le métal fondu est déposé couche après couche. Ce procédé s’est fortement développé depuis 2020.
- le MBJ (Metal Binder Jetting), une nouvelle variante, consiste à projeter des gouttes de liants sur un lit de poudre métallique pour l’agglomérer, puis à passer la pièce dans un four de frittage ; le liant est alors brûlé et la pièce consolidée. L’avantage est que l’impression se fait à température ordinaire, et que l’on peut en faire des centaines en même temps : c’est la voie conduisant aux grandes séries.
Les applications
Les applications sont nombreuses.
Beaucoup de petites pièces d’électroménager sont fabriquées en plastique (polyéthylène, rilsan, nylon). Une fois le logiciel d’impression configuré, les imprimantes alimentées par des bobines de résines fonctionnent toutes seules ; la main d’œuvre est réduite ainsi que les coûts de fabrication. Dans les années 2000, la baisse des prix sur les imprimantes grand public de 200 € à 600 € et la possibilité de mutualiser des scanners 3D et des logiciels d’impression gratuits ont multiplié les « fab lab » dans les établissements d’enseignement ou les maisons de la culture. Après quelques années d’emballement, la FA s’est plutôt développée dans l’industrie et le « hobby » est devenu un épiphénomène.
En métallurgie et en matériaux composites, de nombreuses industries l’utilisent soit en sous-traitant à des ateliers spécialisés en FA, soit en interne pour des pièces complexes comme les hélices creuses pour les bâtiments de Naval Group fabriquées par WAAM ; ceci permet de réduire les stocks et les délais d’approvisionnement. Autre exemple : Constellium, le leader français sur l’aluminium commercialise une poudre d’aluminium Aheadd® CP1 étudiée spécialement pour les pièces des bolides de F1.
Dans le sport (3), pour la chaussure tout terrain de rugby et de football « Shark ONE », la semelle, les renforts et la forme ont été imprimés en 3D en PA11 (polyamide 11 ou rilsan) et Pebax® (constitué de blocs de polyamide et de polyéther), des matières éco-responsables de la société Arkema.
En défense, l’armée américaine a développé des mini-usines qui se déplacent sur le terrain avec des imprimantes 3D pour la fabrication de pièces cassées ou manquantes dans l’armement des armées sur le front. En Ukraine, des drones civils ont été modifiés pour porter des charges et de l’armement.
On se rappelle qu’au milieu des années 2000 un logiciel et les données 3D ont été mis sur le Net par un étudiant américain permettant de fabriquer un révolver presque en totalité en plastique et tirant de vraies balles. En 2025, les spécialistes de la lutte anti-terroriste nous mettent en garde sur la facilité et la disponibilité de telles fabrications sur la toile ou sur les réseaux sociaux à des fins criminelles.
Dans le domaine médical, l’extrapolation du prototypage rapide utilisé depuis plus de 30 ans a été un réel progrès pour l’odontologie et la chirurgie. À l’aide des images de l’IRM, on peut fabriquer des prothèses sur mesure et précises, même complexes (mâchoires, articulations de hanches, genoux…) assez rapidement et parfois en temps réel.
On est près de la science-fiction quand on parle d’impression d’organes humains.
Une société lyonnaise s’appuyant sur des découvertes du CNRS imprime de la peau (4). On prépare d’abord la bio-encre avec des cellules de peau, de la gélatine, un peu d’alginate et de fibrinogène. On passe ensuite à l’impression sur un support en atmosphère stérile puis dans un incubateur durant 21 jours. On imprime ensuite le derme par-dessus avec la même encre. Cette peau imprimée peut servir aux essais des firmes biopharmaceutiques pour les crèmes et cosmétiques, évitant les tests sur animaux.
La construction n’est pas en reste. La fabrication additive permet de construire des bâtiments. Un très beau projet réalisé en 2024 sur les composites résine–bois regroupant deux industriels de la charpente et de la FA, en collaboration avec l’École du Bois d’Épinal et l’École d’Architecture de Nancy ,vise à réaliser la première machine de « stratoconception » de 20 à 30 mètres pour des halls ou salles de sports.
Quels défis pour la FA ?
L’impression plastique continue à se développer mais elle doit tenir compte du recyclage des fils polymères dans une démarche d’économie circulaire menée par les chimistes. Les procédés de la FA sont ceux qui ont le moins d’impacts sur l’environnement, moins de matière, pas de déchets. Mais lors de la conception des logiciels d’impression, les algorithmes de l’intelligence artificielle peuvent optimiser les structures des pièces à fabriquer, en vue de performances spécifiques. Cette nouvelle application de l’IA commence à diffuser.
Le dernier défi à relever concerne la formation et le recrutement car on demande de plus en plus de compétences (5) dans ce domaine où chimie, polymères et matériaux sont les mots-clés pour cette industrie 4.0. Des salons sont consacrés à l’impression 3D où des acteurs du secteur présentent leurs réalisations et recrutent, comme le salon 3D Print à Lyon, par exemple.
Jean-Claude Bernier et l’équipe Question du mois
Pour en savoir plus
(1) La 3D, troisième révolution industrielle ?, J.-Cl. Bernier L'Actualité Chimique (juillet 2015)
(2) Le Laser en contexte industriel : une palette d’applications étonnantes, T. Engel, Colloque Chimie et lumière, Fondation de la Maison de la Chimie (février 2020)
(3) Le rôle des matériaux composites dans les performances sportives, Y. Rémond, Colloque Chimie et Sports en cette Année Olympique et Paralympique, Fondation de la Maison de la Chimie (février 2024)
(4) L’impression fait peau neuve, J. Leyes et B.Robert, Grand Prix Jeunes Journalistes de la Chimie 2018 (vidéo et article)
(5) Voir l’Espace Métiers de Mediachimie
Crédit illustration : capture vidéo L’impression fait peau neuve, J. Leyes et B.Robert, Grand Prix Jeunes Journalistes de la Chimie 2018
Vidéo du mois : Eva Ekeblad et la pomme de terre
Le 10 juillet 1724, en Suède, nait Eva de La Gardie, plus connue sous le nom de son époux Eva Ekeblad. Elle côtoie les paysans, cherche un moyen de lutter contre les famines et propose de généraliser la culture de la pomme de terre. Cette dernière a été introduite en Suède en 1658 par le naturaliste Olof Rudbeck (1630-1702) dans le jardin botanique d’Uppsala.
Mediachimie a créé pour vous des vidéos passionnantes et riches d’informations sur des anecdotes historiques relatives à la chimie. Retrouvez chaque mois une nouvelle vidéo.
Le 25 mars dernier, le jury du Grand Prix des Jeunes Journalistes de la Chimie (GPJJC) s'est réuni et a procédé à la sélection des 4 binômes de l’édition 2025 du concours, parmi un total de 17 dossiers de candidature.
Les 4 dossiers retenus sont :
- La Paléoprotéomique. Maël BREHONNET - Athéna SALHI-IJBA - Institut de Journalisme de Bordeaux Aquitaine
- Les parfums de synthèse. Élisa LENGLART--LECONTE - Élisa MARUENDA - École de Journalisme de Grenoble - ELISAS_EJDG
- Remplacer le sucre : l’édulcorant idéal existe-t-il ? Emma BARETS - Adèle LEBRUN - Institut pratique du journalisme (IPJ) de Dauphine PSL
- Détruire les PFAS grâce à la chimie. Arthur BAUDIN - Noé MEGEL - Institut français de presse (IFP-Panthéon-Assas)
La prochaine étape sera la rencontre avec le jury le 9 avril prochain à la Fondation, puis deux mois d’investigations pour produire un article et une vidéo.
Rendez-vous en juin pour visionner et lire les productions et surtout connaître le binôme vainqueur du GPJJC 2025 (remise des grands prix le 26 juin à la Fondation de la Maison de la chimie).
Pour information, ci-dessous les membres du Jury :
Françoise BELLANGER
Chaine L’esprit Sorcier TV
Vincent BORDENAVE
Le Figaro - Sciences et Médecine
Carole CHATELAIN
Journaliste Scientifique
Alain COINE
Ancien Délégué Général d’Universcience Partenaires
Bernard MEUNIER
Directeur de recherche émérite au CNRS,
Membre et ex-Président de l’Académie des sciences et membre de l’Académie Nationale de Pharmacie
Danièle OLIVIER
Présidente du Jury
Vice-Présidente de la Fondation de la Maison de la Chimie
Jean-Marc SIGOT
Journaliste scientifique, réalisateur, auteur Chaine L’esprit Sorcier TV
Yann VERDO
Les Echos - Chef de rubrique Science
Philippe WALTER
Vice-Président Fondation de la Maison de la Chimie
Membre de l’Académie des Sciences
Tout d’abord qu’est-ce que le tartre ? Tartre et calcaire sont synonymes et tous les deux constitués de carbonate de calcium de formule chimique CaCO3, c’est-à-dire formés à partir des ions calcium Ca2+ et des ions carbonates CO32-.
Le carbonate de calcium est très présent dans la nature, dans les terrains dit calcaires : Bassin parisien, Nord, Alpes, Jura, Champagne crayeuse..., comme le montre la figure 1.
L’eau qui pénètre dans ces sols dissout une partie des sels présents et s’enrichit ainsi en sels minéraux avant d’atteindre les nappes phréatiques d’où elle sera pompée puis traitée et rendue potable.
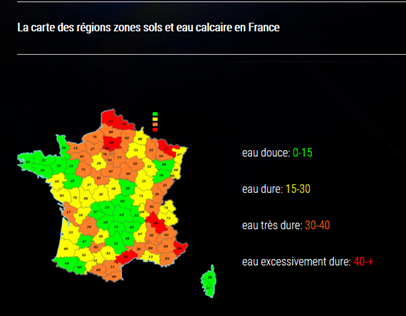
Figure 1 (i)
On définit la « dureté » de l'eau, paramètre qui mesure la quantité d’ions calcium et magnésium, présents dans l'eau. Elle s’exprime en degré TH (°f), pour Titre Hydrotimétrique français.
1 degré TH(°f ) = 4 mg de Ca2+ ou 2,4 mg de Mg2+ par litre d’eau.
On attribue les adjectifs « douce » ou « dure » aux eaux selon la valeur de ce TH.
Échelle (ii)
Notons que dans un terrain calcaire, l’eau s’est enrichie simultanément en ions calcium et carbonate.
Influence du pH sur les ions carbonates
Les ions carbonates participent à des équilibres acido-basiques, comme le montre la figure 2.
Le dioxyde de carbone CO2 est un acide faible et se transforme pour pH supérieur à 6,35 en ion hydrogénocarbonate (aussi appelé ion bicarbonate). Celui-ci se transforme en ion carbonate pour pH supérieur à 10,3.
L’eau du robinet a un pH compris entre 7,2 et 7,6. Il en est de même des eaux en bouteille non gazeuses. A ce pH, l’eau dure contient donc des ions calcium et des ions majoritairement sous forme d'hydrogénocarbonate et non de carbonate (cf. figure 2).

L’équilibre des espèces carbonatées dans l’eau
En réalité les trois espèces coexistent et sont toujours en équilibre dans l’eau, selon :
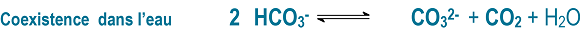
Dire que le bicarbonate est majoritaire c’est dire que les ions CO32- et le dioxyde de carbone CO2 sont très minoritaires mais présents.
Au final l’eau dure contient donc des ions calcium et des ions hydrogénocarbonates, qui restent dissous.
Que se passe-t-il quand on chauffe l’eau ?
Le chauffage de l’eau va favoriser le dégazage de CO2 dont la solubilité dans l’eau diminue si la température augmente. Cela va provoquer naturellement un déplacement de l’équilibre précédent vers la droite pour reformer du CO2. Mais il se forme donc simultanément des ions carbonate. Or les ions carbonates et les ions calcium ont une affinité l’un pour l’autre et vont précipiter sous forme de carbonate de calcium. La réaction qui a lieu est la suivante :
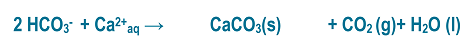
Le tartre s’est formé !
C’est la raison pour laquelle vous observez un dépôt de calcaire tout particulièrement sur les résistances de chauffe-eau, de lave-linge, de lave-vaisselle, dans les cafetières, dans les fers à repasser… Cela engendre des dépenses d’énergie supplémentaires, limite l’efficacité des savons et détergents, le linge est rêche…
Comment peut-on éviter ou éliminer ces dépôts ?
Comme nous l’avons vu (figure 2), les ions carbonates sont des bases donc l’action d’un acide va détruire le calcaire. C’est le rôle des détartrants ou du vinaigre que vous pouvez utiliser. La réaction qui a lieu est
CaCO3 + 2 H+ → Ca2+ + CO2 (gaz) + H2O
Evidemment on ne peut pas mettre un détartrant directement au cours d’un cycle de lave-linge ou de lave-vaisselle. Dans ce cas on peut adoucir l’eau en remplaçant les ions calcium par les ions sodium, c’est le rôle du « sel régénérant », constitué de chlorure de sodium pur (NaCl). On peut aussi ajouter à la lessive un composé qui réagit sur les ions calcium (on parle de séquestration ou de complexation) les empêchant de précipiter avec les ions carbonates(iii).
Pour limiter l’entartrage des résistances de chauffe-eau, on peut adoucir l’eau en amont de l’installation.
Consommation d’une eau dure
Boire une eau dure ne pose aucun problème de santé. Bien au contraire : n’oublions pas que l’ion calcium a une grande importance physiologique (os, dents) et qu’il participe au fonctionnement de la cellule et à la contraction musculaire. L’ion magnésium participe à de très nombreux processus biologiques, au bon fonctionnement du système nerveux et son apport est exclusivement nutritionnel.
On prendra soin de ne pas boire l’eau adoucie riche en ions sodium, car une consommation en excès de ces ions peut entraîner de l'hypertension artérielle.
Françoise Brénon
(i) Source https://la-meilleure-centrale-vapeur.fr/le-calcaire/
(ii) Source https://fr.wikipedia.org/wiki/Duret%C3%A9_de_l%27eau
(iii) ce sont souvent des tensioactifs anioniques de type carboxylate : RCOO- à longues chaine carbonée (R). Cela peut aussi être des hexamétaphosphates de sodium (Na6P6O18).
Crédit illustration : Résistance chauffe-eau, F. Brénon.
La gomme xanthane est connue du grand public comme additif alimentaire présent dans de très nombreuses préparations culinaires industrielles, pour ses propriétés épaississantes, stabilisantes et d’amélioration de la texture. Elle a aussi beaucoup d’autres applications.
C’est un polysaccharide, biopolymère synthétisé naturellement par la bactérie Xanthomonas campestris, non pathogène pour l'homme. Cette bactérie est responsable de maladies pour certains végétaux, comme le chou : la substance qu'elle synthétise obture les pores des feuilles. L’étude des propriétés remarquables de cette substance a conduit à produire la gomme xanthane, utilisée depuis 1960 […]
Accédez au Zoom sur la gomme xanthane
Crédit illustration : AB-7272 / Adobe Stock