 |
Comment réalise-t-on l’impression 3D ou fabrication additive ?
|
Comment réalise-t-on l’impression 3D ou fabrication additive ?
Rubrique(s) : Question du mois

L’impression 3D encore appelée couramment Fabrication Additive (FA) a quitté le domaine du prototypage dans les années 1980 pour gagner le domaine industriel et même le domaine ludique après les années 2000. Elle consiste à réaliser des pièces en 3 dimensions par ajouts successifs de couches de matières principalement des polymères ou des métaux. Elle s’oppose donc à la fabrication soustractive dont le principe est de retirer de la matière à une pièce préalablement moulée (1).
Elle présente de multiples avantages : elle repousse les limites de la technologie en réalisant des formes complexes jusqu’ici irréalisables par moulage ou forgeage, elle permet d’optimiser la quantité de matière première et donc de réduire les coûts et elle permet aussi de réduire les déchets.
Quels sont les procédés de Fabrications Additives ?
Le principe repose sur celui des imprimantes à jet d’encre que l’on retrouve dans tous les bureaux, sauf qu’ici on ne projette plus d’encre chargée en noir de carbone mais un polymère fondu ou une poudre métallique. De même, la buse de projection ne se promène plus de droite à gauche au-dessus du papier (2D), mais elle est animée d’un mouvement vertical au-dessus d’un plateau qui bouge horizontalement (3D).
- FDM (Fused Deposition Modelling) est le procédé le plus connu. L’imprimante est alimentée par un filament de moins d’un millimètre de diamètre d’un thermoplastique qui passe dans une buse chauffée à environ 150° à 250°C. Commandés par un logiciel qui contient les données géométriques de l’objet à fabriquer, les mouvements du plateau et de la buse construisent l’objet couche après couche. Des bobines de fils de PLA (acide polylactique) biodégradable, d’ABS (acrylonitrile butadiène styrène) ou de PET (polyéthylène téréphtalate basse et haute densité) sont maintenant disponibles très couramment chez les industriels des polymères et en 2009 l’expiration des brevets FDM popularise cette technique et lui donne un fort développement.
- Autres types de procédés dérivés du FDM :
- FTI (Film Transfer Imaging) utilise un photopolymère ; après dépôt on illumine avec des lampes infrarouges ou un laser UV pour durcir les couches de résine (SLA StéreoLithography Apparatus) ;
- MJM (Modelage à Jets Multiples) dispose de plusieurs buses et des arrivées de mélanges pour avoir des couches de polypropylène et d’acrylates ;
- SLS (Selective Laser Sintering) quitte le domaine des polymères pour la métallurgie. Des couches successives de poudres de métal (aluminium, acier, titane…) sont déposées et sont frittées par un laser IR de puissance (2). Avec les brevets sur le SLS qui ont expiré en 2014, nombre d’entreprises se sont lancées avec des ateliers entiers d’imprimantes à la fabrication de pièces complexes en petites séries pour l’automobile, l’aéronautique et le spatial.
- Autres types dérivés du SLS :
- le SLM (Selective Laser Melting) : on fait fondre à haute température le fil métallique et on dépose des couches de métal fondu.
- le WAAM (Wire Arc Additive Manufacturing) est un peu une déviation de la soudure à l’arc, puisque le fil est une électrode mise en fusion par arc électrique et le métal fondu est déposé couche après couche. Ce procédé s’est fortement développé depuis 2020.
- le MBJ (Metal Binder Jetting), une nouvelle variante, consiste à projeter des gouttes de liants sur un lit de poudre métallique pour l’agglomérer, puis à passer la pièce dans un four de frittage ; le liant est alors brûlé et la pièce consolidée. L’avantage est que l’impression se fait à température ordinaire, et que l’on peut en faire des centaines en même temps : c’est la voie conduisant aux grandes séries.
Les applications
Les applications sont nombreuses.
Beaucoup de petites pièces d’électroménager sont fabriquées en plastique (polyéthylène, rilsan, nylon). Une fois le logiciel d’impression configuré, les imprimantes alimentées par des bobines de résines fonctionnent toutes seules ; la main d’œuvre est réduite ainsi que les coûts de fabrication. Dans les années 2000, la baisse des prix sur les imprimantes grand public de 200 € à 600 € et la possibilité de mutualiser des scanners 3D et des logiciels d’impression gratuits ont multiplié les « fab lab » dans les établissements d’enseignement ou les maisons de la culture. Après quelques années d’emballement, la FA s’est plutôt développée dans l’industrie et le « hobby » est devenu un épiphénomène.
En métallurgie et en matériaux composites, de nombreuses industries l’utilisent soit en sous-traitant à des ateliers spécialisés en FA, soit en interne pour des pièces complexes comme les hélices creuses pour les bâtiments de Naval Group fabriquées par WAAM ; ceci permet de réduire les stocks et les délais d’approvisionnement. Autre exemple : Constellium, le leader français sur l’aluminium commercialise une poudre d’aluminium Aheadd® CP1 étudiée spécialement pour les pièces des bolides de F1.
Dans le sport (3), pour la chaussure tout terrain de rugby et de football « Shark ONE », la semelle, les renforts et la forme ont été imprimés en 3D en PA11 (polyamide 11 ou rilsan) et Pebax® (constitué de blocs de polyamide et de polyéther), des matières éco-responsables de la société Arkema.
En défense, l’armée américaine a développé des mini-usines qui se déplacent sur le terrain avec des imprimantes 3D pour la fabrication de pièces cassées ou manquantes dans l’armement des armées sur le front. En Ukraine, des drones civils ont été modifiés pour porter des charges et de l’armement.
On se rappelle qu’au milieu des années 2000 un logiciel et les données 3D ont été mis sur le Net par un étudiant américain permettant de fabriquer un révolver presque en totalité en plastique et tirant de vraies balles. En 2025, les spécialistes de la lutte anti-terroriste nous mettent en garde sur la facilité et la disponibilité de telles fabrications sur la toile ou sur les réseaux sociaux à des fins criminelles.
Dans le domaine médical, l’extrapolation du prototypage rapide utilisé depuis plus de 30 ans a été un réel progrès pour l’odontologie et la chirurgie. À l’aide des images de l’IRM, on peut fabriquer des prothèses sur mesure et précises, même complexes (mâchoires, articulations de hanches, genoux…) assez rapidement et parfois en temps réel.
On est près de la science-fiction quand on parle d’impression d’organes humains.
Une société lyonnaise s’appuyant sur des découvertes du CNRS imprime de la peau (4). On prépare d’abord la bio-encre avec des cellules de peau, de la gélatine, un peu d’alginate et de fibrinogène. On passe ensuite à l’impression sur un support en atmosphère stérile puis dans un incubateur durant 21 jours. On imprime ensuite le derme par-dessus avec la même encre. Cette peau imprimée peut servir aux essais des firmes biopharmaceutiques pour les crèmes et cosmétiques, évitant les tests sur animaux.
La construction n’est pas en reste. La fabrication additive permet de construire des bâtiments. Un très beau projet réalisé en 2024 sur les composites résine–bois regroupant deux industriels de la charpente et de la FA, en collaboration avec l’École du Bois d’Épinal et l’École d’Architecture de Nancy ,vise à réaliser la première machine de « stratoconception » de 20 à 30 mètres pour des halls ou salles de sports.
Quels défis pour la FA ?
L’impression plastique continue à se développer mais elle doit tenir compte du recyclage des fils polymères dans une démarche d’économie circulaire menée par les chimistes. Les procédés de la FA sont ceux qui ont le moins d’impacts sur l’environnement, moins de matière, pas de déchets. Mais lors de la conception des logiciels d’impression, les algorithmes de l’intelligence artificielle peuvent optimiser les structures des pièces à fabriquer, en vue de performances spécifiques. Cette nouvelle application de l’IA commence à diffuser.
Le dernier défi à relever concerne la formation et le recrutement car on demande de plus en plus de compétences (5) dans ce domaine où chimie, polymères et matériaux sont les mots-clés pour cette industrie 4.0. Des salons sont consacrés à l’impression 3D où des acteurs du secteur présentent leurs réalisations et recrutent, comme le salon 3D Print à Lyon, par exemple.
Jean-Claude Bernier et l’équipe Question du mois
Pour en savoir plus
(1) La 3D, troisième révolution industrielle ?, J.-Cl. Bernier L'Actualité Chimique (juillet 2015)
(2) Le Laser en contexte industriel : une palette d’applications étonnantes, T. Engel, Colloque Chimie et lumière, Fondation de la Maison de la Chimie (février 2020)
(3) Le rôle des matériaux composites dans les performances sportives, Y. Rémond, Colloque Chimie et Sports en cette Année Olympique et Paralympique, Fondation de la Maison de la Chimie (février 2024)
(4) L’impression fait peau neuve, J. Leyes et B.Robert, Grand Prix Jeunes Journalistes de la Chimie 2018 (vidéo et article)
(5) Voir l’Espace Métiers de Mediachimie
Crédit illustration : capture vidéo L’impression fait peau neuve, J. Leyes et B.Robert, Grand Prix Jeunes Journalistes de la Chimie 2018
 |
Vidéo Histoire du mois : Eva Ekeblad et la pomme de terre
|
Vidéo Histoire du mois : Eva Ekeblad et la pomme de terre
Rubrique(s) : Événements

Vidéo du mois : Eva Ekeblad et la pomme de terre
Le 10 juillet 1724, en Suède, nait Eva de La Gardie, plus connue sous le nom de son époux Eva Ekeblad. Elle côtoie les paysans, cherche un moyen de lutter contre les famines et propose de généraliser la culture de la pomme de terre. Cette dernière a été introduite en Suède en 1658 par le naturaliste Olof Rudbeck (1630-1702) dans le jardin botanique d’Uppsala.
Mediachimie a créé pour vous des vidéos passionnantes et riches d’informations sur des anecdotes historiques relatives à la chimie. Retrouvez chaque mois une nouvelle vidéo.
Il y a trois cents ans, le 10 juillet 1724, en Suède, nait Eva de La Gardie, plus connue sous le nom de son époux Eva Ekeblad. Elle côtoie les paysans, cherche un moyen de lutter contre les famines et propose de généraliser la culture de la pomme de terre. Cette dernière a été introduite en Suède en 1658 par le naturaliste Olof Rudbeck (1630-1702) dans le jardin botanique d’Uppsala.
En 1746, Eva Ekeblad écrit à l’Académie royale des sciences de Suède afin de présenter les travaux qu’elle a effectués sur la pomme de terre. Cette Académie a été fondée en 1739. Eva Ekeblad a transformé les pommes de terre en farine de pomme de terre et en alcool. Dans sa cuisine, elle a cuit les pommes de terre, les a écrasées puis les a séchées afin d’obtenir une poudre fine comparable à la farine de blé. Cette farine est utilisée en pâtisserie. Eva Ekeblad va aussi faire fermenter puis distiller cette pomme de terre écrasée afin d’obtenir de l’éthanol. Cet alcool va donner de la vodka. Jonas Alströmer (1685-1761) et Jacob Faggot (1699-1777), membres de l’Académie, étudient les travaux et deux ans plus tard, Eva Ekeblad devient la première femme membre de l’Académie royale des sciences de Suède. Ses travaux sont publiés dans les Actes de l’Académie en 1748 sous son nom de jeune fille Eva de La Gardie avec pour titre Tentatives de fabrication de pain, d’eau de vie, d’amidon et de poudre de pomme de terre. Il n’existe aucune trace de sa présence aux réunions de l’Académie et en 1751, elle est qualifiée de membre honoraire car seuls les hommes sont admis. En 1752, dans les Actes de l’Académie, un nouveau texte parait sous son nom de jeune fille « Description du savon adapté au blanchiment du fil de coton ».
Dans les cosmétiques, Eva Ekeblad remplace les produits dangereux par de la farine de pomme de terre. La farine de pomme de terre ne doit pas être confondue avec la farine de fécule de pomme de terre. Pour préparer de la farine de pomme de terre on utilise des pommes de terre entières, la farine a la même composition et le goût de la pomme de terre. La farine de fécule de pomme de terre ne contient que l’amidon de la pomme de terre, elle n’a pas de goût, c’est une poudre légère et qui sert d’épaississant en cuisine.
Eva Ekeblad aurait orné sa coiffure de fleurs de pommes de terre.
Son travail a permis la généralisation de la culture de la pomme de terre, il a réduit les risques de famine et les crises alimentaires.


À gauche : Portrait d'Eva de la Gardie (1724-1786) par Gustaf Lundberg (1695-1786).
À droite : Solanum tuberosum L., Atlas des plantes de France (1891).
Pour en savoir plus
- La pomme de terre et ses variétés, Ministère de l'Agriculture et de la Souveraineté alimentaire
- Eva EKEBLAD, sur le site scientificwomen.net (en anglais)
- Eva Ekeblad, la femme scientifique qui a fabriqué de la vodka à partir de pommes de terre, sur le site postoast.com (en anglais)
Crédits illustrations :
- Portrait d'Eva de la Gardie, source Wikimedia Commons, domaine public.
- Solanum tuberosum L., Atlas des plantes de France (1891), source Wikimedia Commons, domaine public.
Vidéo : Réalisation : François Demerliac ; Auteur scientifique : Catherine Marchal ; Production : Fondation de la Maison de la Chimie / Virtuel
 |
Grand Prix des Jeunes Journalistes de la Chimie : les finalistes en lice
|
Grand Prix des Jeunes Journalistes de la Chimie : les finalistes en lice
Rubrique(s) : Événements

Le 25 mars dernier, le jury du Grand Prix des Jeunes Journalistes de la Chimie (GPJJC) s'est réuni et a procédé à la sélection des 4 binômes de l’édition 2025 du concours, parmi un total de 17 dossiers de candidature.
Les 4 dossiers retenus sont :
- La Paléoprotéomique. Maël BREHONNET - Athéna SALHI-IJBA - Institut de Journalisme de Bordeaux Aquitaine
- Les parfums de synthèse. Élisa LENGLART-LECONTE - Élisa MARUENDA - École de Journalisme de Grenoble - ELISAS_EJDG
- Remplacer le sucre : l’édulcorant idéal existe-t-il ? Emma BARETS - Adèle LEBRUN - Institut pratique du journalisme (IPJ) de Dauphine PSL
- Détruire les PFAS grâce à la chimie. Arthur BAUDIN - Noé MEGEL - Institut français de presse (IFP-Panthéon-Assas)
La prochaine étape sera la rencontre avec le jury le 9 avril prochain à la Fondation, puis deux mois d’investigations pour produire un article et une vidéo.
Rendez-vous en juin pour visionner et lire les productions et surtout connaître le binôme vainqueur du GPJJC 2025 (remise des grands prix le 26 juin à la Fondation de la Maison de la chimie).
Pour information, ci-dessous les membres du Jury :
Françoise BELLANGER
Chaine L’esprit Sorcier TV
Vincent BORDENAVE
Le Figaro - Sciences et Médecine
Carole CHATELAIN
Journaliste Scientifique
Alain COINE
Ancien Délégué Général d’Universcience Partenaires
Bernard MEUNIER
Directeur de recherche émérite au CNRS,
Membre et ex-Président de l’Académie des sciences et membre de l’Académie Nationale de Pharmacie
Danièle OLIVIER
Présidente du Jury
Vice-Présidente de la Fondation de la Maison de la Chimie
Jean-Marc SIGOT
Journaliste scientifique, réalisateur, auteur Chaine L’esprit Sorcier TV
Yann VERDO
Les Echos - Chef de rubrique Science
Philippe WALTER
Vice-Président Fondation de la Maison de la Chimie
Membre de l’Académie des Sciences
 |
Pourquoi se forme-t-il du tartre sur les résistances chauffantes ? Et peut-on l’éviter ?
|
Pourquoi se forme-t-il du tartre sur les résistances chauffantes ? Et peut-on l’éviter ?
Rubrique(s) : Question du mois

Tout d’abord qu’est-ce que le tartre ? Tartre et calcaire sont synonymes et tous les deux constitués de carbonate de calcium de formule chimique CaCO3, c’est-à-dire formés à partir des ions calcium Ca2+ et des ions carbonates CO32-.
Le carbonate de calcium est très présent dans la nature, dans les terrains dit calcaires : Bassin parisien, Nord, Alpes, Jura, Champagne crayeuse..., comme le montre la figure 1.
L’eau qui pénètre dans ces sols dissout une partie des sels présents et s’enrichit ainsi en sels minéraux avant d’atteindre les nappes phréatiques d’où elle sera pompée puis traitée et rendue potable.
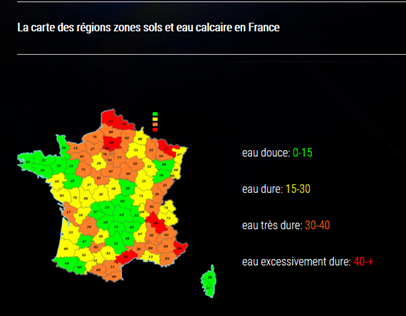
Figure 1 (i)
On définit la « dureté » de l'eau, paramètre qui mesure la quantité d’ions calcium et magnésium, présents dans l'eau. Elle s’exprime en degré TH (°f), pour Titre Hydrotimétrique français.
1 degré TH(°f ) = 4 mg de Ca2+ ou 2,4 mg de Mg2+ par litre d’eau.
On attribue les adjectifs « douce » ou « dure » aux eaux selon la valeur de ce TH.
Échelle (ii)
Notons que dans un terrain calcaire, l’eau s’est enrichie simultanément en ions calcium et carbonate.
Influence du pH sur les ions carbonates
Les ions carbonates participent à des équilibres acido-basiques, comme le montre la figure 2.
Le dioxyde de carbone CO2 est un acide faible et se transforme pour pH supérieur à 6,35 en ion hydrogénocarbonate (aussi appelé ion bicarbonate). Celui-ci se transforme en ion carbonate pour pH supérieur à 10,3.
L’eau du robinet a un pH compris entre 7,2 et 7,6. Il en est de même des eaux en bouteille non gazeuses. A ce pH, l’eau dure contient donc des ions calcium et des ions majoritairement sous forme d'hydrogénocarbonate et non de carbonate (cf. figure 2).

L’équilibre des espèces carbonatées dans l’eau
En réalité les trois espèces coexistent et sont toujours en équilibre dans l’eau, selon :
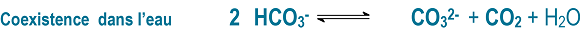
Dire que le bicarbonate est majoritaire c’est dire que les ions CO32- et le dioxyde de carbone CO2 sont très minoritaires mais présents.
Au final l’eau dure contient donc des ions calcium et des ions hydrogénocarbonates, qui restent dissous.
Que se passe-t-il quand on chauffe l’eau ?
Le chauffage de l’eau va favoriser le dégazage de CO2 dont la solubilité dans l’eau diminue si la température augmente. Cela va provoquer naturellement un déplacement de l’équilibre précédent vers la droite pour reformer du CO2. Mais il se forme donc simultanément des ions carbonate. Or les ions carbonates et les ions calcium ont une affinité l’un pour l’autre et vont précipiter sous forme de carbonate de calcium. La réaction qui a lieu est la suivante :
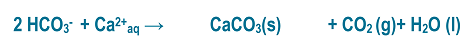
Le tartre s’est formé !
C’est la raison pour laquelle vous observez un dépôt de calcaire tout particulièrement sur les résistances de chauffe-eau, de lave-linge, de lave-vaisselle, dans les cafetières, dans les fers à repasser… Cela engendre des dépenses d’énergie supplémentaires, limite l’efficacité des savons et détergents, le linge est rêche…
Comment peut-on éviter ou éliminer ces dépôts ?
Comme nous l’avons vu (figure 2), les ions carbonates sont des bases donc l’action d’un acide va détruire le calcaire. C’est le rôle des détartrants ou du vinaigre que vous pouvez utiliser. La réaction qui a lieu est
CaCO3 + 2 H+ → Ca2+ + CO2 (gaz) + H2O
Evidemment on ne peut pas mettre un détartrant directement au cours d’un cycle de lave-linge ou de lave-vaisselle. Dans ce cas on peut adoucir l’eau en remplaçant les ions calcium par les ions sodium, c’est le rôle du « sel régénérant », constitué de chlorure de sodium pur (NaCl). On peut aussi ajouter à la lessive un composé qui réagit sur les ions calcium (on parle de séquestration ou de complexation) les empêchant de précipiter avec les ions carbonates(iii).
Pour limiter l’entartrage des résistances de chauffe-eau, on peut adoucir l’eau en amont de l’installation.
Consommation d’une eau dure
Boire une eau dure ne pose aucun problème de santé. Bien au contraire : n’oublions pas que l’ion calcium a une grande importance physiologique (os, dents) et qu’il participe au fonctionnement de la cellule et à la contraction musculaire. L’ion magnésium participe à de très nombreux processus biologiques, au bon fonctionnement du système nerveux et son apport est exclusivement nutritionnel.
On prendra soin de ne pas boire l’eau adoucie riche en ions sodium, car une consommation en excès de ces ions peut entraîner de l'hypertension artérielle.
Françoise Brénon
(i) Source https://la-meilleure-centrale-vapeur.fr/le-calcaire/
(ii) Source https://fr.wikipedia.org/wiki/Duret%C3%A9_de_l%27eau
(iii) ce sont souvent des tensioactifs anioniques de type carboxylate : RCOO- à longues chaine carbonée (R). Cela peut aussi être des hexamétaphosphates de sodium (Na6P6O18).
Crédit illustration : Résistance chauffe-eau, F. Brénon.
 |
La gomme xanthane, E415
|
La gomme xanthane, E415
Rubrique(s) : Zoom sur...

La gomme xanthane est connue du grand public comme additif alimentaire présent dans de très nombreuses préparations culinaires industrielles, pour ses propriétés épaississantes, stabilisantes et d’amélioration de la texture. Elle a aussi beaucoup d’autres applications.
C’est un polysaccharide, biopolymère synthétisé naturellement par la bactérie Xanthomonas campestris, non pathogène pour l'homme. Cette bactérie est responsable de maladies pour certains végétaux, comme le chou : la substance qu'elle synthétise obture les pores des feuilles. L’étude des propriétés remarquables de cette substance a conduit à produire la gomme xanthane, utilisée depuis 1960 […]
Accédez au Zoom sur la gomme xanthane
Crédit illustration : AB-7272 / Adobe Stock
Les différentes filières de formation en chimie selon le bac obtenu sont présentées ainsi que les passerelles.
Organisation de la vidéo/ conférence
- 0:00 Introduction
- 1:40 Pourquoi choisir la chimie ?
- 2:26 Que permet l’expertise des chimistes ?
- 5:33 Vue d’ensemble des parcours de formation
- 6:15 De Bac à Bac +2/3 les filières vers une sortie en tant que technicien ou technicienne
- 6:46 Les différents BTS à l’issue d’un bac général, STL et bac pro
- 10:42 Licence Pro
- 12:02 Les différents BUT à l’issue d’un bac général ou STL
- 14:26 Les licences L1 à L3
- 16:45 Par l’apprentissage
- 17:08 Exemples de métiers de techniciens et techniciennes
- 19:12 De bac à bac + 5/8 vers une sortie en tant qu’ingénieur(e) ou docteur(e)
- 19:13 Vue d’ensemble
- 20:04 La voie CPGE à l’issue d’un bac général - concours à Bac + 2
- 23:31 La voie CPGE TPC à l’issue d’un bac STL concours à Bac + 2
- 24:11 La voie CPI (5 Classes Préparatoires Intégrées) à l’issue d’un bac général – contrôle continu
- 25:46 Les 20 écoles d’ingénieurs de chimie et de génie chimique de la Fédération Gay-Lussac
- 26:28 La voie CITI à l’école de chimie de Rennes à l’issue d’un bac STL - contrôle continu
- 27:12 Les masters
- 29:04 Les passerelles vers les écoles d’ingénieurs de chimie et de génie chimique à partir de BUT, BTS ou L3
- 31:11 Les écoles à cursus intégrés à l’issue d’un bac général ou technologique
- 33:11 Exemples de domaines d’activités en entreprise et de métiers
- 34:22 Présentation de quelques pages de Mediachimie relatives aux métiers
- 36:10 Répartition des ingénieur(e)s chimistes par secteurs industriels et économiques
- 38:13 Liens Internet
- 39:29 Conclusion
Le support de la présentation en PDF est disponible ci-dessous.
Source : Vidéo Conférence Enregistrée au Village de la Chimie 2025
 |
Après le chocolat… la mousse au chocolat !
|
Après le chocolat… la mousse au chocolat !
Rubrique(s) : Événements

Après une première vidéo sur la chimie du chocolat et de ses arômes, voici maintenant une vidéo sur les mystères de la mousse au chocolat.
À travers cette vidéo de Blablareau au labo, coproduite avec Mediachimie et la Fondation de la Maison de la Chimie, découvrez comment obtenir une mousse gouteuse, ferme et stable.
La gomme xanthane est connue du grand public comme additif alimentaire présent dans de très nombreuses préparations culinaires industrielles, pour ses propriétés épaississantes, stabilisantes et d’amélioration de la texture. Elle a aussi beaucoup d’autres applications.
C’est un polysaccharide, biopolymère synthétisé naturellement par la bactérie Xanthomonas campestris, non pathogène pour l'homme. Cette bactérie est responsable de maladies pour certains végétaux, comme le chou : la substance qu'elle synthétise obture les pores des feuilles. L’étude des propriétés remarquables de cette substance a conduit à produire la gomme xanthane, utilisée depuis 1960.
Structure chimique
Hétéropolysaccharide(i) de très haute masse moléculaire(ii), la structure primaire de la gomme xanthane est une chaîne principale de cellulose(iii), c’est-à-dire un enchaînement de monomères β-D-glucose liés entre eux(iv) et présentant tous les 2 glucoses, un branchement latéral de 3 sucres comme le montre la figure 1. Ce branchement est chargé négativement. Les contre-ions de cette chaîne anionique sont essentiellement Na+, K+, Ca2+. La masse d'une unité de répétition est Mw = 982 g.mol-1.
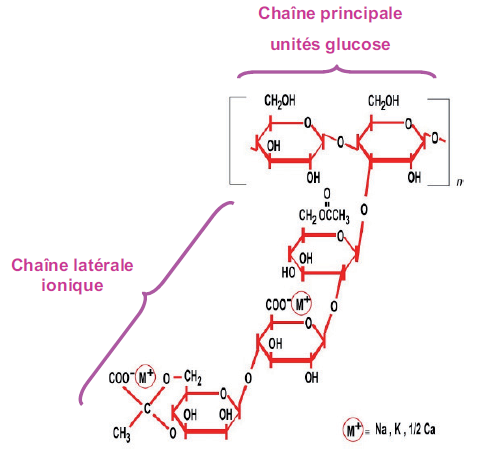
Figure 1 – source [4] page 90
Propriétés physico-chimiques
La gomme xanthane est soluble dans l’eau à froid (dès 10 à 20˚C), insoluble dans les solvants organiques et supporte les hautes températures (80-100°C). La gomme présente des groupements hydroxyles et des charges négatives qui facilitent l’interaction soluté-eau. De plus, les ramifications écartent les chaînes principales, ce qui facilite l’hydratation.
La viscosité de la gomme xanthane en solution aqueuse relève de la rhéologie(v). Ses propriétés sont celles d’un fluide thixotrope : au-dessous d’une certaine contrainte de cisaillement, les bâtonnets rigides de gomme sont stabilisés par des interactions faibles, ils ne peuvent s'agiter et le liquide devient visqueux ; cette viscosité des solutions de gomme diminue avec des taux de cisaillement élevés (si on secoue, mélange, mastique...). Lorsque les forces de cisaillement sont supprimées, le mélange s'épaissit à nouveau. Par exemple, dans la vinaigrette, l'ajout de gomme xanthane la rend suffisamment épaisse pour qu'elle reste homogène au repos dans la bouteille. Mais les forces de cisaillement créées en secouant et en versant la fluidifient, permettant de la verser aisément. Au sortir de la bouteille, les forces de cisaillement sont supprimées, et le mélange s'épaissit et adhère aux feuilles de salade !
Propriétés biologiques
La gomme résiste à la dégradation par la plupart des enzymes : les liaisons β (1->4) de la cellulose sont déjà résistantes et les chaînes latérales les rendent plus difficiles d'accès.
Elle est très peu digestible(vi) (non assimilable par le système digestif humain), du fait que sa chaîne principale est une cellulose. Ainsi, sa valeur énergétique potentielle(vii) est de 16 720 kJ/kg (4 000 kcal/kg) mais sa valeur réelle n’est que de 2 500 kJ/kg (600 kcal/kg).
La gomme n'a pas de goût et n'altère pas les propriétés organoleptiques des milieux où on l'introduit. Elle est réputée non toxique, est approuvée dans l'industrie agro-alimentaire depuis 1969 aux USA et 1974 dans la CEE, sous le numéro E415 [1][2].
Applications
Contrairement à certains polysaccharides végétaux (guar et caroube surtout) qui varient selon l'origine et la période de récolte, le procédé industriel d’obtention de la gomme xanthane est bien maîtrisé et les qualités du produit sont constantes. Par ailleurs, si on veut obtenir des variations de propriétés du produit recherché, il est plus facile de modifier une souche bactérienne qu'une plante.
Suivant les pays, elle est autorisée dans différentes applications à des doses allant généralement de 0,1 à 1 % (en masse) et autorisée sans restriction dans les applications cosmétiques.
Sur le marché alimentaire [1][3], on la trouve pour ses propriétés épaississantes, gélifiantes et stabilisatrices, dans des préparations de sauces, vinaigrettes industrielles, soupes instantanées, desserts lactés, produits surgelés, viennoiseries… Elle stabilise les composés en suspension comme les morceaux de fruits, les mousses, les crèmes et yaourts. Elle permet également la suspension de particules d’épices et d’exhausteurs de goût. Cela permet de compenser certains ingrédients trop chers, difficiles à mettre en œuvre, détruits lors des opérations ou efficaces mais trop caloriques, comme les graisses, ou les sucres ou l'amidon. Sa non-digestibilité est un avantage.
Elle peut aussi être employée comme substitut du gluten. Elle est compatible avec les régimes végétaliens, végétariens(viii), halal et casher(ix) .
Dans l’industrie pharmaceutique, elle est utilisée comme agent épaississant et comme ingrédient dans les formulations protectrices. Elle est également employée pour retarder la libération de la substance active du comprimé. Elle est utilisée pour la nutrition des personnes dysphagiques, avec des eaux épaissies. En outre, elle permet de créer de la salive artificielle, pour traiter les personnes souffrant du syndrome de Sjögren(x).
Dans l’industrie cosmétique, la gomme xanthane est utilisée comme stabilisateur, émulsifiant, épaississant et gélifiant dans les dentifrices, les gels, les shampoings, les crèmes et les lotions. Elle améliore la viscosité et aide à maintenir la consistance des produits. Dans les crèmes elle joue aussi un rôle d’hydratant en formant un film à la surface de la peau qui limite l'évaporation de l'eau et la déshydratation.
Dans l’industrie du pétrole et du gaz, elle a une utilisation importante en grandes quantités, comme fluide de forage pour maximiser la récupération du pétrole.
Autres usages : elle est utilisée comme ingrédient dans les peintures, les teintures textiles, les fongicides, les engrais, les détergents et les adhésifs. Dans le BTP, elle facilite le mélange et la projection des ciments et mortiers.
Production
La production industrielle de gomme xanthane se fait dans de gros fermenteurs (jusqu’à plusieurs centaines de mètres cubes) puissamment agités. Le procédé est le plus souvent discontinu (batch)(1). Le milieu de fermentation comprend essentiellement :
- une source de carbone : amidon, sucres, mélasse ;
- une source azotée : soja, ammoniaque ;
- l’oxygène de l’air ;
- des enzymes.
Les bactéries produisent le polymère pour se protéger lorsqu'elles sont en condition de stress ; il faut donc choisir des conditions favorables à la croissance bactérienne pour qu'elles soient stressées ! mais pas trop. Au cours de la fermentation qui peut durer plusieurs dizaines d’heures le milieu devient visqueux ce qui pose des problèmes délicats d’agitation et de refroidissement du fermenteur. Température et pH sont des paramètres importants. Le moussage est parfois difficile à contrôler. La stérilisation de l’équipement est clé de la réussite.
En fin de fermentation, le moût est stérilisé à haute température pour tuer les microorganismes et dénaturer les enzymes présentes. La gomme est alors précipitée à l'isopropanol qui sera recyclé. La partie du procédé qui suit la fermentation appelé DSP (Down Stream Processing) est complexe ; elle met en jeu les opérations unitaires de filtration, séchage, broyage, tamisage parfois granulation. Le procédé utilise de grandes quantités d’eau qu’il faut traiter. On obtient in fine une poudre jaune pâle ou blanche qui peut se conserver plusieurs années.
La production mondiale dépasse les 30 000 tonnes /an (1). C’est le polysaccharide microbien, c’est-à-dire biosynthétisé naturellement par une bactérie, le plus vendu.
Le marché de la gomme Xanthane devrait passer de 754,8 millions USD (environ 700 millions d'euros) en 2024 à 996,3 millions USD en 2029 (environ 900 millions d'euros), avec un taux de croissance annuel de 5,71 % [3].
En conclusion, la gomme xanthane a un bel avenir, facilite les opérations culinaires et fournit des produits dont la conservation est excellente. Elle n'est pas toxique et est hypocalorique puisque non digérée.
Cependant, en cas de consommation importante et fréquente, bien que non assimilée par l'homme, elle pourrait être impliquée dans la prise de poids. Son usage depuis un demi-siècle a amené pour certaines personnes le microbiote intestinal à s'adapter, certaines bactéries auraient muté, et deux d'entre elles seraient associées pour dégrader la gomme xanthane [5] : l'une la décomposerait en ses monosaccharides, que l'autre transformerait en acides gras qui, eux, sont bien assimilés par l’organisme ! Cela prouve que nous devons ne pas abuser des produits multi-transformés et varier notre alimentation pour éviter de donner l'occasion à notre microbiote de nous jouer des tours...
Nicole Moreau et l’équipe Zoom sur…
(i) Le préfixe hétéro indique qu'il y a divers sucres dans le polymère. Sinon, on dirait homopolysaccharide
(ii) Sa masse moléculaire est de 1,5 x 106 à 5 x 106 Dalton soit par mole de 1500 à 5000 g mol-1.
(iii) La chaine principale présente un enchainement d’environ 10 000 à 20 000 oses [4].
(iv) Les monomères β-D-glucose sont liés entre eux par liaison O-glycosidique (1->4). Cette chaîne porte tous les 2 glucoses un branchement latéral triosidique. Ce branchement est constitué d’un α-D-mannose lié à la chaîne principale par liaison osidique (1->3), d’un acide β-D-glucuronique lié au 1er mannose par liaison osidique (1->2) et d’un β-D-mannose lié à l’acide glucuronique par liaison osidique (1->4). Le 1er mannose est le plus souvent acétylé en position 6 et le 2e mannose peut être pyruvylé par liaison cétalique en positions 4 et 6.
(v) La rhéologie est l'étude de la déformation et de l'écoulement de la matière sous l'effet d'une contrainte appliquée.
(vi) C’est à dire qu’elle n’est pas digérée et donc éliminée à l'extérieur de l'organisme par le gros intestin.
(vii) C'est l'énergie stockée dans les liaisons chimiques d'une substance.
(viii) Elle remplace la gélatine ou les œufs.
(ix) En effet la gomme xanthane peut être utilisée comme substitut du collagène, qui lui, provient de la peau et des os des bœufs et des porcs.
(x) Sécrétion salivaire insuffisante
Références
[1] Gomme xanthane : agent viscosant et stabilisant, J.-L. Simon, Procédés chimie-bio-agro | Agroalimentaire, Techniques de l’Ingénieur (2001)
(2) [2] Gomme xanthane, sur le site Ataman Chemicals
[3] [3] Rapport mondial : Aperçu du marché de la Gomme de Xanthan 2025, sur le site de Foodcom Experts
[4] [4]Des additifs pour texturer des aliments, M. Desprairies, La chimie et l’alimentation (EDP Sciences, 2010) p. 83 - 99
[5] [5]Mechanistic insights into consumption of the food additive xanthan gum by the human gut microbiota, M. P. Ostrowski, Nature Microbiology 7(4):556-56, sur le site de PubMed/National Library of Medecine
Crédit illustration : AB-7272 / Adobe Stock
Pour faire suite à la vidéo sur la chimie du chocolat, découvrons maintenant les ressorts de la mousse au chocolat. Au fur et à mesure de la réalisation en direct de la mousse au chocolat, vous sont expliqués le choix des ingrédients, leurs rôles et les interactions qui vont être mises en jeu entre eux pour obtenir une mousse gouteuse, ferme et stable.
La vidéo se présente en plusieurs parties
- 0:00 Introduction et Ingrédients de la recette
- 1:30 Fusion du chocolat et rôle d’un ajout éventuel de beurre
- 6:20 Séparations des blancs et des jaunes des œufs et rôles de chacun d’eux.
- 9:50 Ppourquoi les protéines du blanc d’œuf stabilisent la mousse et éventuel ajout d’un peu d’eau
- 13:30 Évolutions de la recette avec ajouts de jaune d’œuf et de sucre, et pourquoi.
- 15:50 Mélange
- 16:50 Dégustations, impressions, conclusion
Production : Association LABOXYGENE, Fondation de la Maison de la chimie

