Synthèse du bleu indigo et découverte de ses propriétés. Un film de la série Lumia et les catalyseurs.
De belles images pour illustrer les réactions d’oxydo-réduction oscillant autour de l’état d’équilibre : réactions de Briggs-Rauscher et de Belooussov-Jabotinski.
Source : Palais de la Découverte, hébergé sur le site www.canal-u.tv
Introduites par un bref exposé sur la définition des termes chaleur, température, ébullition et évaporation, trois expériences sont réalisées pour expliquer les différents états de la matière - état solide, liquide et gazeux - et donner à voir les changements d'un état à l'autre.
Un grand classique du Palais de de la découverte avec des expériences concrètes, vivantes et spectaculaires. Une bonne illustration pour les cours de thermodynamique sur les changements d’état du corps pur.
Source : Palais de la découverte,hébergé sur le site www.canal-u.tv
Les propriétés surprenantes de l'air liquide et de divers matériaux refroidis (caoutchouc, métaux, mercure, iodure mercurique, soufre, feuille d’arbre…) à très basse température - durcissement, fragilisation, transformation allotropiques, effet sur les organismes biologiques - nous sont présentées, ainsi que la distillation de l'air liquide. Des applications industrielles sont citées.
Un très grand classique qui a émerveillé de nombreux visiteurs au Palais de la découverte. Permet de revoir ces expériences impossibles à réaliser dans les laboratoires des lycées.
Source : Palais de la Découverte, hebergé sur le site www.canal-u.tv
On sait aujourd’hui fabriquer des matériaux légers et résistants mais pouvant être refaçonnés à température élevée et ceci de manière réversible. Cette très courte communication propose de très belles photos des objets réalisés.
Un nouveau matériau révolutionnaire façonnable à chaud comme du verre (lien externe)
Source : CNRS, communiqué de presse, 15 novembre 2011
Ce long article très riche et très bien structuré fait un état des lieux de la chimie des matériaux, non seulement la synthèse mais aussi l’analyse et les procédés d’élaboration des matériaux. Ceux-ci sont utilisés non seulement pour ce qui concerne l’énergie (que ce soit pour de la conversion, du stockage, ou dans le domaine de l’énergie nucléaire), mais aussi l’habitat, l’information et la communication, ou la santé.
Chimie des matériaux - Nanomatériaux et procédés (PDF, lien externe)
Source : Rapport de conjoncture 2010 du comité national du CNRS
 |
Pourquoi et comment les feuilles se colorent en automne et tombent en hiver ?
|
Pourquoi et comment les feuilles se colorent en automne et tombent en hiver ?
Rubrique(s) : Question du mois

Qui dans sa vie n’a pas vu en automne le jeu des couleurs magnifiques des feuilles de la majorité des arbres qui nous entourent ? Jaune de toutes les nuances, orange, rouge feu, rouge byzantin…
En effet l’arbre, n’ayant pas des moyens de déplacement, ne peut s’abriter pendant les mois rudes de l’hiver. Il a donc développé sa propre stratégie de survie contre le gel.
Il préfère sacrifier ses feuilles, celles qui occupent le plus de surface exposée, pour se protéger de la dessiccation et garder ses branches, tronc et racines. L’ensemble des structures restantes est protégée soit par l’écorce (branches et tronc) soit par la terre (racines).
La chimie de la chute
Aussitôt que la luminosité baisse et que les premiers froids paraissent, l’arbre, grâce à des molécules senseurs (réceptrices), va réaliser la venue de l’hiver ; l’ordre va être donné pour secréter une petite molécule hormone qui s’appelle éthylène (1), molécule bien connue par ailleurs de l’industrie pétrochimique.
La biosynthèse de l’éthylène va alors se réaliser grâce à une succession complexe d’étapes chimiques à partir de la méthionine (2), qui est un acide aminé essentiel pour la constitution des protéines.
L’éthylène va déclencher un deuxième mécanisme, celui de fabrication de « liège » autour des veinules ou artérioles qui amènent la sève (le sang des arbres) vers le feuillage pour le nourrir et l’hydrater ; un « bouchon » est formé qui empêche l’alimentation des feuilles (3). L’avenir de ces feuilles dépend désormais du vent… L’hiver s’installe mais la chimie de l’arbre lui a encore sauvé la vie, pour une nouvelle année.
Les changements de couleur
La chlorophylle (4), cette molécule responsable de la couleur verte intense et qui assure le processus de la photosynthèse (5), va être progressivement dégradée par le froid.
Le vert disparait pour laisser place à d’autres colorants, cachés jusqu’alors par la couleur verte. Ce sont les caroténoïdes (6) (substances chimiques de la carotte) ou les anthocyanines (substances chimiques des choux).
La danse des couleurs est amorcée ; tous les jours, à chaque instant de la journée et en fonction de la luminosité, des nuances variées régalent nos yeux.
Pourquoi certains arbres ne perdent pas leur feuillage ?
Le cas des conifères en est un exemple didactique.
Leur feuillage en forme d’aiguilles diminue substantiellement la surface d’exposition. Par ailleurs, il s’agit d’arbres résineux qui laissent autour de chaque aiguille une fine couche de résine qui sert de vêtement de protection, comparable à la cire secrétée par les canards qui nagent dans l’eau, indifféremment de la température ambiante.
La stratégie des plantes est une source d’émerveillement ! (7)
Constantin Agouridas, Françoise Brénon et l'équipe Question du mois de Mediachimie
(1) Éthylène ou éthène H2C=CH2
(2) La méthionine existe sous 2 structures, images l’une de l’autre dans un miroir. Par exemple la S-méthionine a pour formule :
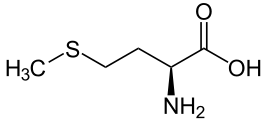
(3) Ce processus s’appelle l’abscission.
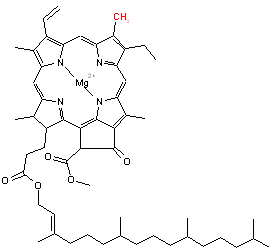
(5) Dans le processus de photosynthèse, la chlorophylle absorbe l’énergie solaire afin de permettre au dioxyde de carbone et à l’eau, présents dans l’air ambiant, de se combiner pour produire des hydrates de carbone (sucre) et libérer du dioxygène.
(6) Caroténoïdes : Il s’agit d’une famille contenant environ 600 molécules différentes. Elles ont en commun de présenter une longue alternance de simples et doubles liaisons, responsable de leur couleur. Par exemple le lycopène a pour formule :
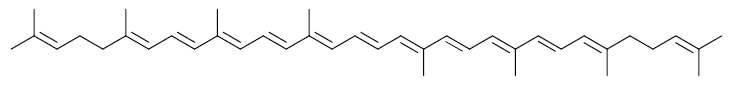
(7) C’est ainsi que certains arbres sécrètent de l'éthylène et d'autres gaz pour empêcher la végétation d'envahir leurs pieds et que sous stress thermique les arbres émettent de l'éthylène, d'où l'inflammation rapide et spectaculaire de l'arbre entier lors des incendies de forêt.
Le problème de la vaccination est rappelé : on signale que seulement 75% des médecins généralistes ont confiance en la vaccination, que le taux couverture vaccinale du personnel de santé est dramatiquement faible, et que plus d’un tiers de la population française se défie des vaccins tout en les jugeant importants et efficaces. Les personnes âgées de plus de 65 ans ne bénéficient d’une protection qu’à hauteur de 35% par rapport à celle des plus jeunes. C’est tout le défi des adjuvants dont l’action doit stimuler ou même créer une immunité du patient vis-à-vis des pathogènes visés.
Les adjuvants les plus utilisés sont ceux de l’aluminium (III). C’est le dépôt du complexe Al-antigène qui est à l’origine de la réaction immunitaire qui se propage lentement dans les liquides interstitiels de l’organisme. Le problème de la tolérance de l’aluminium, la question des maladies auto-immunes pouvant être induites, la recherche d’autres adjuvants sont présentés. La conclusion est qu’aucun lien de causalité avec les adjuvants aluminiques n’a pu être établi à ce jour, Il est donc nécessaire de poursuivre les recherches sur les mécanismes d’action des adjuvants aluminiques.
Source : L'Actualité chimique n° 416 (mars 2017) pp. 8-10
Les couleurs sont une manifestation des interactions rayonnements-matières, lumière / pigments par exemple. L’auteur cite en illustration les peintures pariétales découvertes dans les grottes d’Ardèche peintes grâce à deux pigments : noir pour le charbon et ocre pour les oxydes de fer. D’autres couleurs furent obtenues plus tard : bleu, vert, en jouant sur les états d’oxydation du fer (+3 ou +2) ou en utilisant des minéraux comme la pierre lapis-lazuli. L’alliance des pigments minéraux et de l’art du feu conduit aux verres colorés, les nanoparticules d’or aux curieuses couleurs changeantes de la coupe de Lycurgue. L’émaillage des céramiques, la recristallisation partielle des verres permettent de découvrir les phénomènes de réflexion et de diffusion de la lumière.
Comment jouer avec le feu et la lumière pour colorer les verres et les céramiques (lien externe)
Source : L'Actualité chimique n° 396 (mai 2015) pp. 25-28
L’auteur nous entraîne vers des horizons qui nous font découvrir comment naissent les couleurs. Elles n’existent que dans notre cerveau. Il faut cependant de la lumière car ce sont les photons réfléchis qui frappent notre rétine et déclenchent des réactions biochimiques qui transmettent des signaux à notre cerveau, informations différentes suivant la fréquence de l’onde. À une longueur d’onde correspond une couleur.
Sont traitées la trilogie des couleurs, la couleur liée à la nature chimique des molécules, la couleur « physique » due à un phénomène de l’optique physique et enfin les verres dopés par des nanoparticules de couleurs variables. D’autres classes de lumières colorées sont celles de l’incandescence et celles de la luminescence caractérisées l’une par la température d’émission, et l’autre par la hauteur de l’état excité. Des références nombreuses complètent cet article très compréhensible.
La genèse des couleurs, un dialogue entre lumière et matière (lien externe)
Source : L'Actualité chimique n° 396 (mai 2015) pp. 29-33
