Chimie et Notre-Dame : Présentation du colloque
Après l’incendie de Notre-Dame de Paris qui, en 2019, nous a tous bouleversés, le Ministère de la Culture et le CNRS se sont mobilisés au côté de l’Établissement public chargé de la conservation et de la restauration de la cathédrale Notre-Dame de Paris créé par l’État et se sont associés dans le cadre d’un grand chantier scientifique pour mettre les compétences et les connaissances des chercheurs d’une cinquantaine de leurs laboratoires au service de la « résurrection » de l’édifice et de ses œuvres d’art. À cette occasion, ces chercheurs se sont aussi donné pour objectif le renouvellement des connaissances sur l’édifice et son histoire.
La chimie est présente aussi bien sur le chantier de restauration que dans ce programme de recherche et d’innovation qui associe archéologues, historiens de l’art, chimistes, physiciens et informaticiens, aux architectes et compagnons présents sur le site.
La Fondation de la Maison de la Chimie a souhaité faire le point sur ce que les sciences de la chimie ont et pourront apporter dans le programme de restauration de la cathédrale et plus généralement via des innovations dans le domaine des matériaux du patrimoine. Le responsable et les coordinateurs du programme nous ont fait l’honneur non seulement d’intervenir comme conférenciers, mais aussi de nous aider dans le choix des experts pour réaliser cet ambitieux objectif. Nous les en remercions vivement. La vue de l’incendie de Notre-Dame de Paris et son triste bilan ont profondément touché les citoyen de tous âges dans le monde entier.
Ce colloque, qui vise à apporter des informations précises sur le rôle possible des sciences « chimiques » dans la réparation de ce terrible événement et comment la chimie peut contribuer à lui redonner vie, est ouvert à tous les publics, avec une attention particulière aux jeunes et au monde éducatif. Le niveau des interventions se veut accessible à tous.
Bernard Bigot
Président de la Fondation internationale de la Maison de la Chimie
et Directeur Général de l’Organisation internationale ITER
Chimie et Chimie et Notre-Dame : Le colloque dans son intégralité

- Retrouvez toutes les vidéos sur Viméo/Fondation de la Maison de la Chimie avec la possibilité de télécharger les vidéos, conférence par conférence
- Regardez toutes les vidéos sur Youtube/Mediachimie
- Lisez la fiche Chimie et… en fiches :
L'incendie de Notre-Dame a-t-il considérablement plombé l'atmosphère parisienne ?
- Télécharger l'ouvrage intégral Chimie et Notre-Dame de Paris (PDF-22118 Ko)
Télécharger l'ouvrage intégral Chimie et Notre-Dame de Paris en PDF - 22118 Ko
Colloque Chimie et Notre-Dame : Conférence par conférence
Conférences plénières d’ouverture
Animateur : Bernard BIGOT
- - Le chantier de Notre-Dame de Paris : état et perspectives
- Général d’armée Jean-Louis GEORGELIN | Représentant spécial du Président de la République et président de l’établissement public chargé de la conservation et de la restauration de la cathédrale Notre-Dame de Paris
voir la vidéo et le résumé | chapitre en PDF - - De la chimie des matériaux à l’alchimie des équipes
- Aline MAGNIEN | Conservatrice générale du patrimoine, Directrice du Laboratoire de Recherche des Monuments historiques, Ministère de la Culture et de la Communication - Pascal LIEVAUX | Conservateur général du patrimoine, délégation à l’inspection, à la recherche et à l’innovation, direction générale des Patrimoines et de l’Architecture
voir la vidéo et le résumé | chapitre en PDF
Table Ronde : Ils travaillent pour Sauver Notre-Dame
Animateur : Marc J. LEDOUX | DRCE Émérite du CNRS
- - La restauration des statues en cuivre de la flèche de la cathédrale Notre-Dame de Paris
- Richard BOYER | Directeur Général SOCRA
voir la vidéo et le résumé | chapitre en PDF - - Charpente de sécurisation des arcs boutants et des voûtes
- Julien Le BRAS | Président Directeur Général Groupe Le Bras Frère
voir la vidéo et le résumé | chapitre en PDF - - Conservation-restauration de peintures polluées par dépôt d’aérosols de plomb
- Marie PARANT | Restauratrice de peintures murales, indépendante - Witold NOWIK | Chimiste, ingénieur de recherche, responsable du pôle Peinture murale et polychromie, Laboratoire de Recherche des Monuments Historiques
voir les vidéos et le résumé | chapitre en PDF
Archéo matériaux
Animateur : Jean-Claude BERNIER | Professeur Émérite de l’Université de Strasbourg
- - Mémoire du bois : apport de la chimie à la connaissance de la charpente carbonisée de Notre-Dame de Paris
- Alexa DUFRAISSE | Chargée de recherche au CNRS, UMR 7209, Archéozologie, archéobotanique : Sociétés, Pratiques et Environnements (ASSPE), CNRS/MNHN, Paris
voir la vidéo et le résumé | chapitre en PDF - - Conservation des maçonneries endommagées par les sels solubles suite à l’incendie de Notre-Dame de Paris en 2019
- Véronique VERGES-BELMIN | Géologue, Ingénieure de recherche, responsable du pôle scientifique Pierre, Laboratoire de recherche des monuments historiques (LRMH)
voir la vidéo et le résumé | chapitre en PDF - - L’apport des analyses chimiques à la connaissance des armatures de fer de Notre-Dame de Paris
- Maxime L’HERITIER | Maître de conférences en histoire médiévale, Université Paris 8, ArScAn CNRS UMR 7041
voir la vidéo et le résumé | chapitre en PDF - - Tracer les plombs de Notre-Dame de Paris par leur signature isotopique et élémentaire.
- Sophie AYRAULT | Directrice de Recherches au CEA, Laboratoire des Sciences du Climat et de l’Environnement (LSCE), Université Paris Saclay
voir la vidéo et le résumé | chapitre en PDF
Innovation et matériaux du patrimoine
Animateur : Philippe WALTER | Laboratoire d’archéologie moléculaire et structurale (UMR 8220 CNRS-UPMC), CNRS-Sorbonne Université
- - La conservation-restauration et la recherche sur les vitraux de la cathédrale Notre-Dame de Paris
- Claudine LOISEL | Ingénieure de recherche, responsable du pôle scientifique Vitrail, Laboratoire de recherche des monuments historiques (LRMH)
voir la vidéo et le résumé | chapitre en PDF - - Notre-Dame de Paris, matériaux et construction
- Rémi FROMONT, ACMH | Covalence Architectes - Pascal PRUNET | Architecte en chef des Monuments Historiques
voir les vidéos et le résumé | chapitre en PDF
Conférence Plénière de clôture
Animateur : Mehran MOSTAFAVI | Université Paris-Saclay / Directeur Adjoint Scientifique INC/CNRS
- - Matériaux du patrimoine, compréhension du passé, prévision du futur. Quelques exemples
- Philippe DILLMANN | Directeur de Recherche - CNRS
voir la vidéo et le résumé | chapitre en PDF
Conception graphique : CB Defretin | Images : © Renato SALERI / MAP / Chantier Scientifique Notre-Dame de Paris / Ministère de la culture / CNRS – © Cyril FRESILLON / IRAMAT / NIMBE / ArScAn / CEA / Chantier Scientifique Notre-Dame de Paris / Ministère de la culture / CNRS – © V. ABERGEL/A. GROS/MAP/MIS/Vassar College/A-BIME/Chantier Scientifique Notre-Dame de Paris/Ministère de la culture/CNRS – © V. ABERGEL/L. DE LUCA/MAP/SRA-DRAC/AGP/MIS/Chantier Scientifique Notre-Dame de Paris/Ministère de la culture/CNRS – © Cyril FRESILLON / AASPE / CNRS Photothèque – © Kévin JACQUOT / MAP / Chantier Scientifique Notre-Dame de Paris / Ministère de la culture / CNRS – © V. ABERGEL/L. DE LUCA/MAP/SRA-DRAC/AGP/Vassar College/MIS/Chantier Scientifique Notre-Dame de Paris/Ministère de la culture/CNRS
Maurice Goldhaber meurt le 11 mai 2011 à Setanket-East Setauket dans le comté de Suffolk situé dans l’état de New York à plus de cent ans puisqu’il était né le 18 avril 1911 à Lemberg dans l’Empire austro-hongrois. Cette ville est, de nos jours, en Ukraine et porte le nom de Lviv.
Après la première guerre mondiale, la famille s’installe à Chemnitz dans l'est de l'Allemagne. À Chemnitz, Maurice Goldhaber fréquente le lycée. Il apprend le latin, le français et l’anglais en plus des matières scientifiques. Il obtient l’abitur, équivalent du baccalauréat, en 1930 et décide d’entreprendre des études de physique à Berlin.
À cette époque, de nombreux physiciens de renom enseignent à Berlin comme Max Planck (1858-1947), Albert Einstein (1879-1955), Max von Laue (1879-1960), Walther Nernst (1864-1941), Erwin Schrödinger (1887-1961), Otto Hahn (1879-1968) et Lise Meitner (1878-1968). Il reste trois ans à l’université à Berlin et trouve le cours de Lise Meitner sur la physique nucléaire très stimulant. C’est dans le cours de von Laue qu’il rencontre Gertrude Scharff (1911-1998) qui deviendra son épouse.
En 1933, avec les recommandations d'Erwin Schrödinger et de Max von Laue, il est accepté par Ernest Rutherford (1871-1937) comme étudiant au laboratoire Cavendish. Ce laboratoire est le département de physique de l’Université de Cambridge, il a été fondé en 1874 et porte le nom d’un physico-chimiste anglais talentueux Henry Cavendish (1731-1810). Rutherford le dirige de 1919 à sa mort en 1937.
Maurice Goldhaber a rapidement apporté sa première contribution majeure lorsqu'il a suggéré à James Chadwick (1891-1974), qui avait découvert le neutron en 1932 que le deutéron pourrait être désintégré par des photons à haute énergie. Ils travaillent ensemble et ils publient en 1934 la première mesure précise de la masse du neutron. Grâce à Chadwick la structure de l’atome a été complétée, le noyau est constitué de charges positives les protons et de charges neutres les neutrons autour sur des trajectoires elliptiques se déplacent des charges négatives les électrons ; l’atome est neutre électriquement, il possède autant de protons que d’électrons. Le deutéron encore appelé deuton est le noyau du deutérium, isotope naturel de l’hydrogène. Il contient un proton et un neutron. Les isotopes d’un même élément chimique possèdent le même nombre de protons et un nombre de neutrons différents.
Ces travaux lui permettent d’obtenir le doctorat en physique à l'Université de Cambridge en 1936. Dans le journal Le Temps du 15 septembre 1936, on peut lire dans la rubrique Causerie scientifique : « Or, tout dernièrement Chadwick et Goldhaber ont ouvert une nouvelle voie en montrant qu’un deuton frappé par les rayons gamma se dédouble en donnant un proton et un neutron. » Les rayons gamma sont un rayonnement électromagnétique d’un photon, ils ont une grande énergie et sont de nos jours utilisés en médecine nucléaire ainsi qu’en imagerie médicale.
N’obtenant pas de poste, il part aux États-Unis en 1938 et accepte un poste de professeur à l'Université de l'Illinois. Il est reconnu comme un expérimentateur créatif dans le domaine nucléaire. Mais Il va quitter l’Illinois car sa femme, Gertrude Scharff Goldhaber ne peut pas obtenir un poste rémunéré. Il part, en 1950, au laboratoire national de Brookhaven car sa femme est embauchée. Ce laboratoire a été créé en 1947 sur le site d’une ancienne base militaire américaine Camp Upton sur Long Island. Il dépend du département de l’énergie des États-Unis et son domaine est la physique nucléaire.
Il détermine en 1968, l’hélicité du neutrino avec Lee Grodzins (1926- ) et Andrew Sunyar (1920-1986). Ils montrent que le neutrino a une hélicité gauche car son spin est orienté dans le sens opposé à son mouvement. Le neutrino est une particule élémentaire électriquement neutre. Le spin est une des propriétés des particules en physique quantique. Il caractérise le moment angulaire intrinsèque. Un électron se déplace autour du noyau de l’atome, il a un moment angulaire orbital, il tourne aussi sur lui-même, c’est le moment angulaire intrinsèque ou spin. Si le spin est entier ou nul, les particules portent le nom de bosons. Si le spin est demi-entier, les particules sont nommées fermions. Les électrons et les neutrinos sont des fermions.
Au nom de la commission de l’énergie atomique des États-Unis, en 1968, il dépose un brevet pour l’invention d’un composé hélium-néon permettant l’étude des interactions du neutrino dans les chambres à bulles. Il dirige le département de physique à partir de 1960 et en 1961, il est nommé directeur, poste qu’il conservera jusqu’en 1973. Avec Edward Teller (1908-2003), il propose le modèle dit Goldhaber-Teller qui décrit la résonance géante dipolaire, celle-ci est due à la vibration groupée des neutrons en opposition à la vibration groupée des protons. La société américaine de physique l’élit président en 1982.
Bien que retraité en 1985, il continue de travailler jusqu’à plus de 90 ans. Sa dernière publication date de mai 2011, elle est écrite avec son fils Alfred. Il a obtenu de nombreux prix. En 1971, le prix Tom Wilkerson Bonner en physique nucléaire lui est attribué. Ce prix existe depuis 1964 en mémoire de Bonner (1910-1961). Il récompense des travaux en physique nucléaire et est décerné tous les ans.
Il reçoit le prix J. Robert Oppenheimer en 1982 attribué par le centre d’études théoriques de l’université de Miami depuis 1969. Robert Oppenheimer (1904-1967) est le père du projet Manhattan qui conduira à la fabrication de la bombe A qui a été utilisée à Hiroshima et à Nagasaki.
Puis en 1983, il reçoit la médaille nationale des sciences. Cette médaille est décernée par le président des États-Unis qui choisit les personnes à récompenser parmi une liste établie par la Fondation nationale scientifique. Elle récompense un travail important dans le domaine des sciences sociales, de la biologie, de la chimie, de l’ingénierie, des mathématiques et de la physique ainsi que des sciences du comportement.
Il obtient le prix Wolf en physique en 1991. Ricardo Wolf (1887-1981) est un inventeur d’origine allemande qui a été ambassadeur de Cuba en Israël et qui a créé une fondation. Depuis 1978, la Fondation Wolf attribue tous les ans en Israël six prix à des personnalités pour des réalisations dans l’intérêt de l’humanité et des relations pacifiques entre les peuples sans considération de nationalité, de religion, de couleur, de sexe ou d’opinion politique. Les prix Wolf récompensent des travaux en agriculture, mathématiques, médecine, chimie, physique et art, ils ne sont pas remis tous les ans. En physique et en chimie, les prix sont justes un peu moins prestigieux que le prix Nobel, souvent les lauréats du prix Wolf obtiennent le prix Nobel dans les années qui suivent.
Enfin, en 1999, le prix Enrico Fermi lui est attribué. Ce prix, décerné par les États-Unis à des scientifiques ayant œuvré dans le domaine de l’énergie, est administré par le département de l’énergie des États-Unis. Une médaille en or à l’effigie d’Enrico Fermi (1901-1954) est remise à celui qui reçoit ce prix.
En 2001, le laboratoire national de Brookhaven crée les bourses Gertrude et Maurice Goldhaber en leur honneur. Ces bourses sont décernées à de jeunes scientifiques qui ont déjà des titres et aussi du talent ainsi que des compétences exceptionnelles et dont les recherches montrent une indépendance d’esprit et une curiosité pour des domaines proches de leur sujet.
En 2008, le laboratoire célèbre le 50e anniversaire de la découverte de l'hélicité des neutrinos en donnant une conférence. Maurice Goldhaber, qui a 97 ans, est présent et monte sur l’estrade afin de présenter son point de vue sur l'avenir de la physique.
En août 2009, il déménage près de son fils, Alfred, un professeur de physique à l'Université Stony Brook. Son travail, bien que plus lent, continue. Avec son fils Alfred, il s'est mis à démontrer l'impraticabilité de remarquer l'hélicité inversée des neutrinos, l’article est publié dans Physics Today en mai 2011.
Maurice Goldhaber décède après une courte maladie le 11 mai 2011. Il a formé de nombreux chercheurs et plusieurs de ses élèves ont obtenu le prix Nobel.
Pour en savoir plus
Maurice Goldhaber, P. D. Bond et L. Grodzins, Physics Today (2011) 64 (10), 65
Maurice Goldhaber - A biographical memoir (PDF), R. P. Crease and A. S. Goldhaber, sur le site de National Academy of Sciences
Revue Scientifique 1/01/1939 p. 122 sur Gallica (BNF)
Illustration : Maurice Goldhaber probablement en 1937 GFHund — Travail personnel / Wikimedia, CC BY 3.0
Dans la région provençale, la garance est cultivée pour donner la couleur garance utilisée en teinture. À Avignon, la chambre de commerce propose un concours en 1858 sur la garance : Trouver un procédé usuel propre à reconnaître d’une manière sûre et facile, dans la Garance et les divers produits qui en dérivent, toute espère d’altération ou de mélange ayant un caractère frauduleux. Jean-Henri Fabre (1823-1915), professeur de physique et de chimie au lycée impérial d’Avignon, entreprend des travaux sur la garancine qui est de la poudre de racine de garance. Ces derniers sont récompensés par la chambre de commerce car il obtient le premier prix.
Dès 1826, Pierre-Jean Robiquet (1780-1840) et Jean-Jacques Colin (1784-1865) étudient la racine de garance et isolent deux colorants l’alizarine et la purpurine.
De 1859 à 1861, Jean-Henri Fabre dépose quatre brevets d'invention touchant à l'analyse des fraudes, mais surtout à l'alizarine pure, qu'il a réussi à extraire. Le 30 juillet 1859, le brevet porte le titre de L’obtention d’une garance épurée, au pouvoir tinctorial accru : la paludine.
Mais, en 1868, alors qu’ils travaillent chez BASF, Carl Graebe (1841-1927) et Carl Liebermann (1842-1914) découvrent l’alizarine synthétique qu’ils obtiennent à partir de l’anthracène tiré du goudron de houille. Un brevet est déposé et l’alizarine est commercialisée dès 1871. À un jour près, William Henry Perkin (1838-1907) réalise la même synthèse. L’alizarine est la 1,2-dihydroxyanthraquinone de formule C14H8O4 et de formule développée :
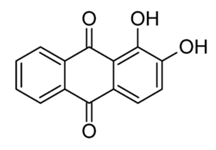
Cette découverte est catastrophique économiquement pour les régions où la garance est cultivée comme la Provence, l’Alsace et la Hollande car l’alizarine synthétique est peu chère et les quantités obtenues sont très importantes. En 1885, l’Allemagne produit en 20 jours autant d’alizarine que le département du Vaucluse et ses environs en une année entière.
Pour Jean-Henri Fabre aussi, c’est une catastrophe car il vient de passer pratiquement dix années à trouver des procédés pour améliorer l’obtention de l’alizarine naturelle et tout ce travail n’aura servi à rien.
C’est ainsi que les soldats français sont partis au combat en août 1914 avec des képis et des pantalons rouges, colorés non plus par la garance issue des cultures françaises mais par l’alizarine produite par l’Allemagne !
Cette tenue historique, nécessaire à la visibilité du soldat sur le champ de bataille enfumé par la poudre noire, devenait un handicap après l’invention de la poudre sans fumée en 1884. Après des tergiversations politiques et idéologiques, il fut décidé qu’il s’agissait maintenant de combattre sans être vu. Ce n’est que fin 1915 que l’intégralité des soldats français a pu disposer de la tenue « bleu horizon » dont le colorant provenait de l’indigo synthétique produit par les Britanniques.
Pour en savoir plus
- Altérations frauduleuses de la garance et de ses dérivés : Mémoires récompensés au concours ouvert à Avignon sur cette question, Chambre de commerce et d'industrie (Avignon), sur le site Gallica (bnf.fr)
- Jean-Henri Fabre, Thèses, Brevets inédits et Mémoires, sur le site e-fabre.com
- L’œuvre de Jean-Henri Fabre, A. Lécaillon, Revue pédagogique (1916) 68-1, pp. 278-297
- L'uniforme du fantassin français en 1914 et 1916, PDF disponible sur le site du Musée de l'Armée-Invalides (rubrique Fiches objets > Dans les collections)
- Rouge garance : une couleur martiale, F. Deherly, Le Blog Gallica (2021)
Illustration : Soldat français de la Première Guerre mondiale en 1914 (in coll. Mémorial de Verdun) Image retouchée (Antonov14)/Wikimedia, licence CC BY-SA 3.0
Nos deux camarades Fadi et Sarah sont de nouveau enfermés dans une pièce du manoir : le grenier. Comme à son habitude, le professeur « Blouseblanche » ne laissera sortir les deux aventuriers que s’ils résolvent la nouvelle énigme qui va leur être proposée. Ainsi, ils pourront déverrouiller le cadenas et visiter d’autres pièces de l’extravagant manoir. Le professeur, toujours accompagné de sa tablette en guise de perroquet sur l’épaule, propose alors aux deux camarades une nouvelle énigme. Sauras-tu leur venir en aide ?
Les différentes utilisations et les supports dédiés
- Pour une résolution utilisant uniquement des supports papier :
- Le livret élève à distribuer (énigme papier)
- Le guide enseignant (énigme papier)
- Pour une résolution mixant supports papier et numérique :
- Le livret élève à distribuer (énigme numérique)
- Le guide enseignant (énigme numérique)
- Les vidéos de présentation de l'énigme et la résolution sont accessibles via un QRcode sur le livret élève
- Les QRcodes des vidéos des indices sont dans le guide enseignant (à imprimer pour distribuer aux élèves si besoin)
L’intelligence artificielle est un des domaines de l’informatique qui prend une place de plus en plus importante dans notre quotidien (moteurs de recherche, itinéraires routiers...) mais aussi dans la recherche depuis quelques décennies. En doublant tous les dix-huit mois, la puissance des ordinateurs n’a cessé d’augmenter de façon très significative au fil des ans. Ceci a permis d’accroître les capacités de ces machines à exécuter des tâches normalement associées à l’être humain pour résoudre, entre autres, des problèmes complexes en analysant des données en nombre de plus en plus colossal. Depuis les années 1960, les chimistes utilisent ces machines capables de traiter des données et les applications liées à leur utilisation permettent d’optimiser la recherche et le développement de nouvelles molécules.
Parties des programmes de physique-chimie associées
- Programme d’enseignement scientifique de terminale, thème 3 :Une histoire du vivant, partie 5 : De la machine de Turing à l’intelligence artificielle
- Programme de la spécialité physique-chimie de terminale générale, partie « Constitution et transformations de la matière », 2.a : Suivre et modéliser l’évolution temporelle d’un système, siège d’une transformation chimique, 4. : Élaborer des stratégies en synthèse organique
- Programme de physique-chimie de terminale STL : partie « Chimie et développement durable » / Synthèses chimiques
- Programme de physique-chimie et mathématiques de première STL : partie « Transformation chimique de la matière » / Cinétique d’une réaction chimique
Les mers et océans représentent 71 % de la surface totale de notre planète pour un volume de près de 1,33 milliard de km3 (soit 98 % des eaux de la planète) et une profondeur moyenne de 3 700 mètres. Contrairement aux écosystèmes terrestres, les écosystèmes marins restent encore très peu explorés : on estime que seulement 5 % des espaces marins ont à ce jour fait l’objet d’études approfondies. Il est vrai que c’est seulement au XXe siècle que l’on a commencé à disposer de technologies et d’équipements adaptés pour explorer les grands fonds (jusqu’à près de –11 500 m dans la fosse des Mariannes). L’extrême diversité de sa faune, sa flore, ses ressources, son potentiel énergétique… font de l’espace marin une réserve de richesses dont on a du mal aujourd’hui à en évaluer l’étendue.
Source : Série Les chimistes dans
L'objectif de la bactérie [1], qui est un procaryote donc dépourvue de noyau (fig. 1), est de se multiplier et « d'occuper le terrain ». C'est d'ailleurs pourquoi de nombreux antibactériens sont produits par des microorganismes, qui éliminent ainsi les concurrents pour être les seuls à disposer des ressources nutritives [2].
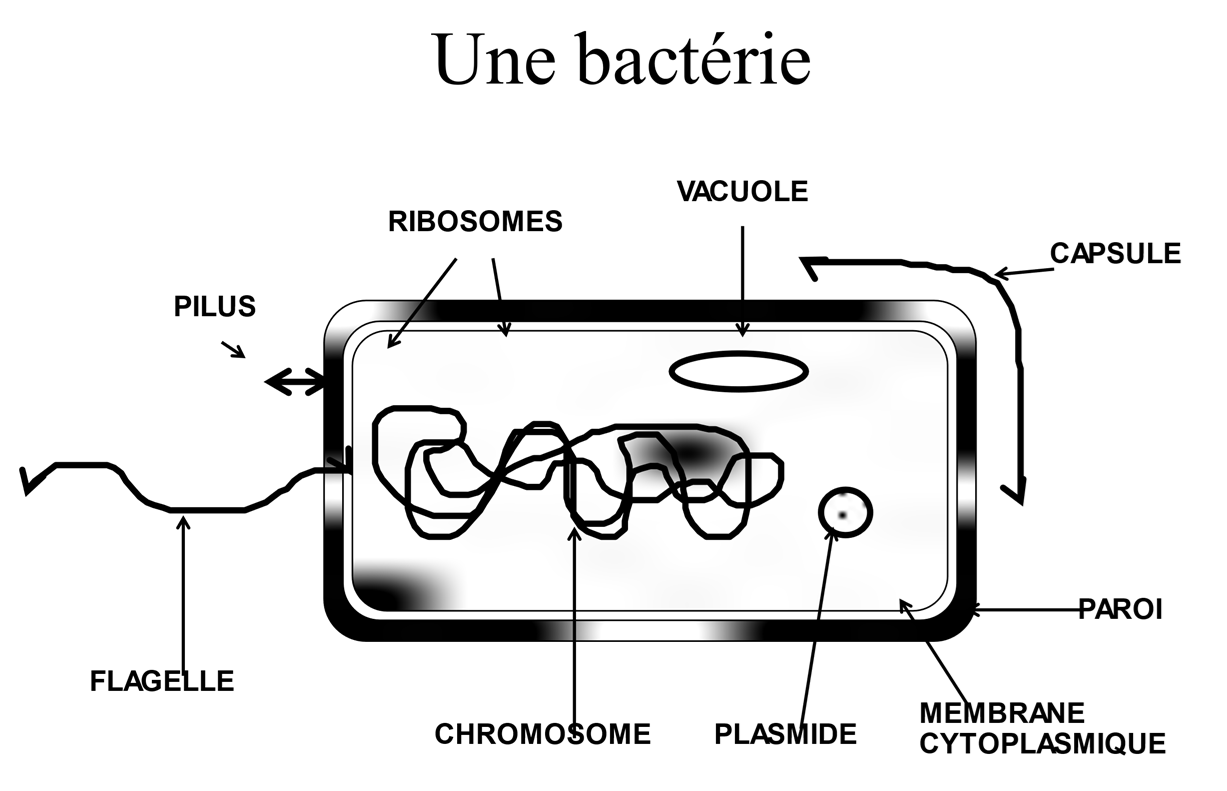
Figure 1
Comme on va le voir, les bactéries savent, depuis toujours, trouver des parades à tout ce qui peut perturber leur développement [3], et en particulier la présence d'agents antimicrobiens.
Elles peuvent devenir Résistantes (R) : la résistance aux antibactériens étant définie comme la capacité d'une bactérie à se multiplier en présence d'une concentration d'antibiotique supérieure à celle que l'on peut obtenir in vivo(i). Cela peut conduire à un échec thérapeutique.
Comment déterminer si une bactérie est sensible ou résistante ?
En cas d'infection persistante malgré un traitement approprié, ou dans les cas graves, le médecin fait un prélèvement(ii) et demande au laboratoire de réaliser un antibiogramme. Le principe est de cultiver la bactérie en présence de divers antibactériens et de voir si elle « pousse » ou si sa croissance est inhibée.
Il existe diverses méthodes plus ou moins automatisées, mais la plus simple à comprendre est d'opérer en boite de Pétri(iii). Sur un milieu nutritif et solide placé à 37°C pendant 15 à 24h les bactéries se développent (fig. 2a). Si avant de mettre à l'étuve on pose sur la boîte des disques de papier imprégnés de quantités standardisées de chaque antibactérien à tester, le diamètre d'inhibition de pousse autour de chaque disque indique le niveau de sensibilité de la souche à l'antibactérien : un contact indique que la résistance est élevée (fig. 2b). Ainsi, la bactérie représentée en jaune est très résistante (R) aux produits 1 et 4, résistante à 5 et sensible (S) à 2 et 3. On appelle Concentration Minimale Inhibitrice ou CMI la concentration d'antibactérien la plus faible pour laquelle il n'y a pas de croissance visible. Cette expérience est une expérience in vitro (fig. 3).
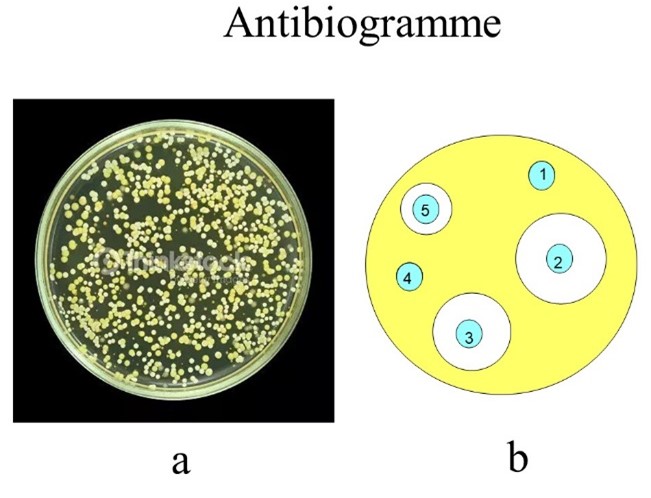
Figures 2a et 2b
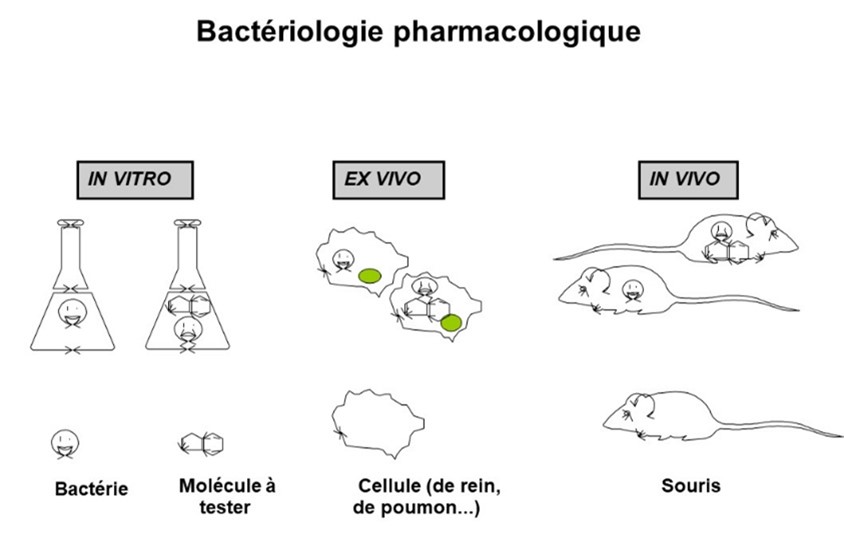
Figure 3
Résistance naturelle
C'est une propriété commune à toutes les bactéries d'une même espèce, due le plus souvent à la nature des enveloppes de la bactérie (fig. 4). Chez les bactéries Gram -, le peptidoglycane est entouré d'une membrane externe asymétrique, dont la partie extérieure, le lipopolysaccharide(iv), empêche la pénétration des molécules hydrophobes à cause de la chaîne de sucres, et celle des hydrophiles à cause de la partie lipidique. Ce n'est que par des canaux emplis d'eau, les porines, que les antibactériens hydrophiles peuvent entrer. Certaines bactéries ont des porines très étroites – c'est le cas des mycobactéries – qui restreignent encore le passage, d’où une résistance importante.
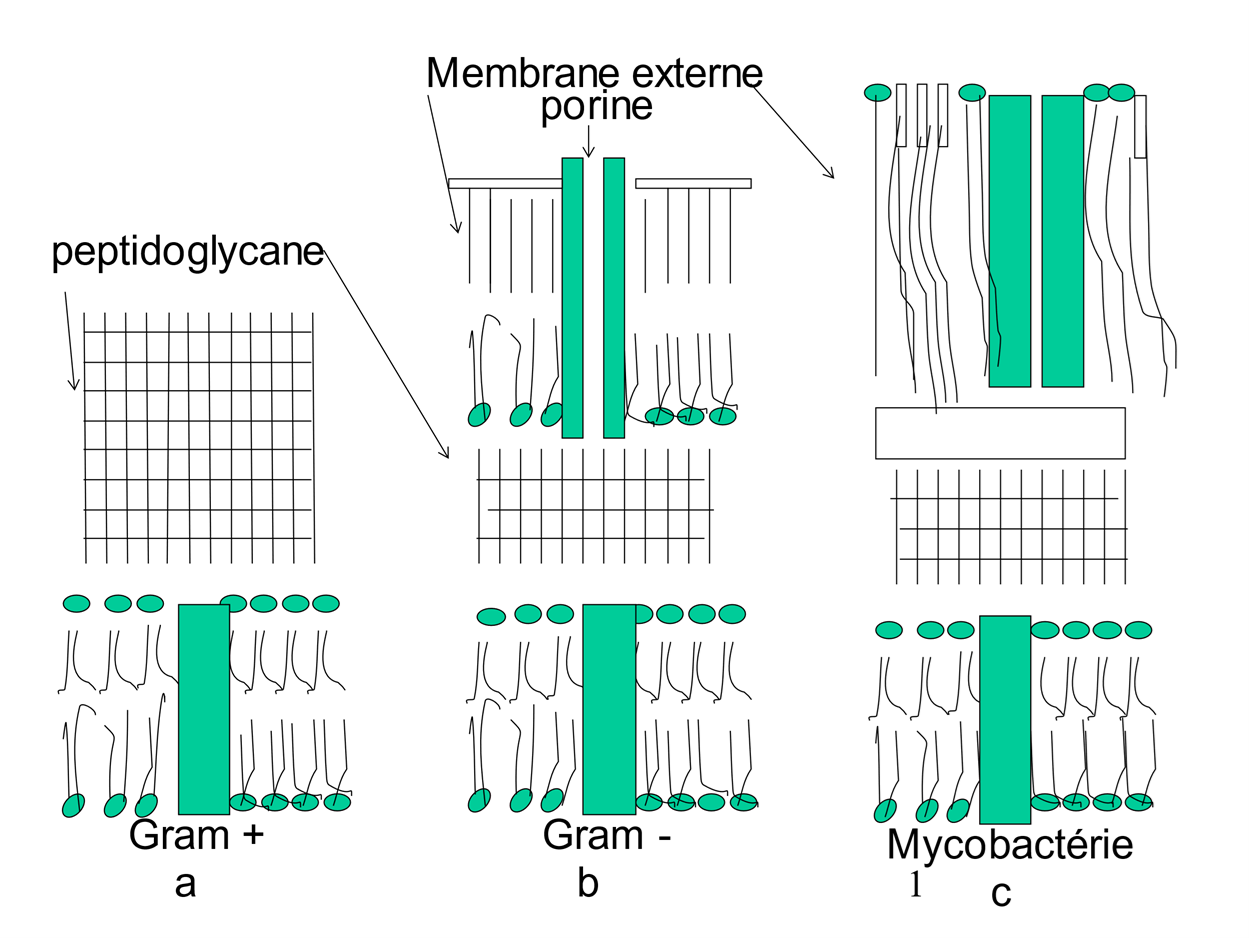
Figure 4
Résistance aux antibactériens
La chimie des médicaments [4] et l’usage des antibactériens a révolutionné la mortalité par infection et à la fin des années 1960, le problème des infections bactériennes semblait résolu. Mais l’évolution naturelle des bactéries dans un environnement contenant des antibactériens les a conduites à développer des mécanismes de résistance, processus accru par l’usage inconsidéré des agents antibactériens. C’est un problème général auquel la France est bien loin d'échapper [5]. Chaque année en Europe, l'antibiorésistance provoque 30.000 morts, et la morbidité est aussi importante que celle de la grippe, de la tuberculose et du VIH/SIDA combinés. À côté du problème de la résistance proprement dite, les conséquences de l'usage accru des antibiotiques sont la multirésistance (une bactérie devient résistante à plusieurs antibactériens de familles différentes), la contamination de l'environnement par les antibactériens et leurs métabolites(v), qui finiront par être ingérés par les humains et les animaux, contaminant encore plus l'environnement. Concernant les antibiotiques donnés aux animaux soit pour raison prophylactique, soit comme stimulant de la croissance, cet usage est interdit en Europe, mais toujours existant aux États-Unis.
Les voyages plus fréquents, les rassemblements, facilitent la dispersion des germes résistants, par simple contact, hors infection. Enfin, les progrès de la médecine ont accru le nombre de personnes fragiles : personnes âgées, immunodéprimées (greffées), pathologies chroniques, porteurs de prothèses... Même la tuberculose, qui semblait éradiquée en France, s'y rencontre à nouveau.
N'oublions pas que la plupart des antibactériens sont d'origine microbienne, ce qui facilite la mise en œuvre de mécanismes de résistance préexistant(vi).
Mécanismes moléculaires de la résistance
Les principaux mécanismes sont schématisés figure 5 :
- empêcher la pénétration de l’antibactérien : modification des porines (Gram -) de la membrane externe
- éjecter l’antibactérien : pompes d’efflux (fig. 6) dans la membrane interne
- modification de l’antibactérien, qui ne sera plus actif : enzymes d’inactivation (fig. 7 pour la pénicilline)
- modification de la cible :
- plus grande quantité de cible, rendant la quantité d'antibactérien insuffisante,
- mutation de la cible, qui ne sera plus reconnue et fonctionnera à nouveau normalement.
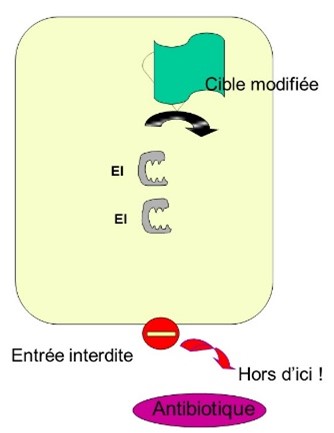 | 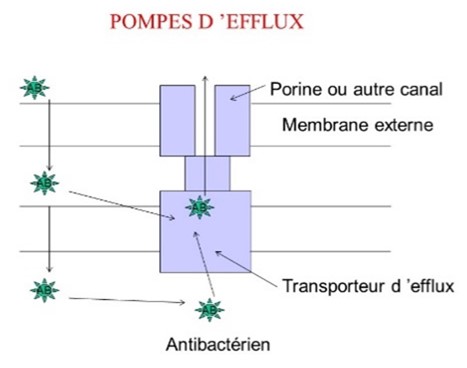 |
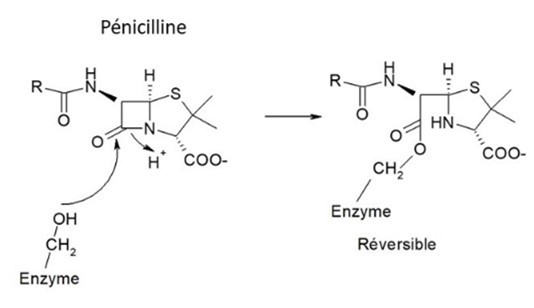
Figure 7
Bases génétiques de la résistance
Toute propriété est codée au niveau de l'ADN. Si le phénomène conduisant à la résistance est porté par le chromosome seuls les bactéries filles sont résistantes(vii).
Mais il existe des éléments mobiles, c'est à dire des fragments d'ADN autres que le chromosome, les plasmides par exemple (fig. 8), qui, s'ils codent pour la résistance, peuvent permettre sa dissémination rapide entre diverses bactéries. La figure10 montre que le plasmide d'une bactérie résistante « bleue » peut se dupliquer, puis une copie est transférée par contact avec une bactérie sensible « jaune », qui deviendra alors résistante.
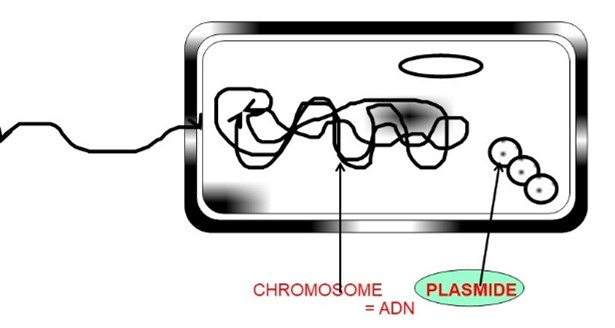
Figure 8
.png)
Figure 9
En conclusion, on voit que le problème de la lutte contre les infections est loin d'être résolu, qu'il faut que patients et prescripteurs sachent être raisonnables en respectant la consigne de la campagne d’information « les antibiotiques, c’est pas automatique », [6] et que l'industrie pharmaceutique ne néglige plus la recherche en antibiothérapie [4] [5].

(i) In vivo : sur un animal vivant ; in vitro : dans un tube à essais; ex vivo : sur un organe ou une cellule isolée.
(ii) Gorge, prélèvement d'urine, de crachat ou intervention plus invasive.
(iii) Du nom du bactériologiste allemand Julius Richard Petri (1852–1921), qui était l'assistant du docteur Robert Koch (découvreur du bacille de la tuberculose) et grand rival de Louis Pasteur : voir le livre « Peste et Choléra » de Patrick Deville.
(iv) Le mot lipopolysaccharide est composé de « lipo » : lipide et "saccharide": sucre.
(v) Quand on donne un médicament à un être vivant, son organisme le transforme (on dit « le métabolise ») en une molécule capable d'être éliminée, appelée métabolite.
(vi) Le producteur d'antibiotique ne doit pas être détruit par les molécules qu'il fabrique !
(vii) Ces bactéries filles coexistent au sein d’une population où il y a d'autres bactéries de même espèce, mais qui n'ont pas développé de résistance.
Pour en savoir plus
[1] Parasite, champignon, bactérie et virus : quelles différences ?, N. J. Moreau, Question du mois, Mediachimie.org (2020)
[2] Zoom sur les bactéries et antibactériens, N. J. Moreau, Zoom sur..., Mediachimie.org (2023)
[3] On regardera avec intérêt Bactéries, nos amies ? CERIMES (1 janvier 1990) Canal-u.tv
[4]Chimie et médicaments : un bel avenir !, B. Meunier, Colloque chimie et nouvelles thérapies (novembre 2019)
[5] Comment vaincre la résistance aux maladies infectieuses ?,B. Meunier, V. Jarlier et Ph. Guérin - article en partenariat Académie des sciences et le Figaro (mai 2013)
[6] Les antibiotiques : des médicaments essentiels à préserver, sur le site de la MGEN (novembre 2022)
Crédits :
- illustration : Image par OpenClipart-Vectors de Pixabay
- figures : © NJ Moreau
La bactérie
Une bactérie [1] est une cellule très simple, « un sac » qui renferme tout ce qui est nécessaire à sa survie (fig. 1).

Figure 1
Il n’y a aucun compartiment et en particulier pas de noyau. C’est ce que l’on appelle un procaryote. Toutes les autres cellules, de la levure de boulanger à nos propres cellules sont des eucaryotes, elles possèdent un noyau [1]. C’est très important, car cela peut permettre de trouver des molécules spécifiques contre les bactéries sans trop de dommages pour les cellules de l’hôte, dont l'ADN est à l'abri dans le noyau.
Ce « sac » est une enveloppe constituée d'une membrane interne, composée essentiellement de lipides, mais dans laquelle peuvent s'insérer des protéines ou d'autres éléments. Elle est protégée par une paroi dont le principal élément est le peptidoglycane. C'est un polymère formé de longues chaînes de sucres pontées par de courtes chaînes peptidiques. On admet qu'il contribue à la forme et la rigidité de la bactérie et protège la membrane interne des effets de la pression osmotique(i). On peut le schématiser comme un gros grillage relativement facile à franchir (fig. 2). La taille d'une bactérie est de l'ordre de 1µm.

Figure 2
Les bactéries sont apparues sur terre il y a 3 milliards d'années(ii). On connaît environ 5000 espèces bactériennes, dont quelques dizaines sont pathogènes. On distingue deux types de bactéries, dites à Gram positif (Gram +) ou à Gram négatif(iii) (Gram -). Les Gram + (fig. 2a) ont une épaisse couche de peptidoglycane. Chez les Gram - (fig. 2b) le peptidoglycane est plus mince, mais est entouré d'une membrane externe complexe et difficile à franchir, sauf par des canaux hydrophiles, les porines, servant à l'entrée des nutriments.
On a aussi les mycobactéries, responsables de la tuberculose, de la lèpre, particulièrement bien protégées par leur enveloppe complexe et riche en lipides (25% environ, contre 1 à 2% pour les autres bactéries) (fig. 2c). En outre, leurs porines sont particulièrement étroites.
L'infection
Les bactéries sont responsables d'infections quand elles pénètrent et se multiplient dans un endroit de l'organisme où elles ne devraient pas être. Cela correspond à une rupture de l’équilibre entre bactérie et moyens de défense de l’hôte. Une infection peut être localisée(iv), locorégionale(v), septicémique(vi). On peut aussi les classer en infections communautaires(vii), et nosocomiales(viii).
L'infection peut être plus ou moins grave selon l'hôte infecté : une banale coupure nettoyée par lavage à l'eau et au savon sera sans conséquence pour un adulte en bonne santé, mais il existe de plus en plus de personnes à risque par suite des progrès de la médecine : personnes de plus en plus âgées, immunodéprimées (ayant subi une greffe par exemple), porteuses de prothèses, souffrant de maladies chroniques... La gravité dépendra aussi de la nature et des propriétés du germe infectieux : faculté d'adhérer aux cellules de l'hôte(ix), excrétion de toxines, capacité de survie dans la cellule infectée...
La lutte contre ces bactéries sera une véritable guerre sans merci, puisque, malgré les nombreuses armes dont nous disposons (les antibactériens), l'ennemi (la bactérie) possède une faculté de dissémination considérable, certaines pouvant se diviser toutes les 20 minutes ! En outre, elle possède plusieurs stratagèmes pour résister à nos armes [2]. Les bactéries communiquent entre elles, et communiquent aussi avec les cellules eucaryotes. Elles sont ainsi capables de maîtriser leur environnement pour y survivre ou s'y multiplier.
Les antibactériens
Quand on parle de la lutte contre les bactéries, il vaut mieux utiliser le terme d'antibactériens, bien spécifique, plutôt que celui plus couramment utilisé d'antibiotiques qui désigne les substances capables de combattre les microbes en général (bactéries, virus, parasites, champignons...). Par définition, les agents antibactériens inhibent la croissance bactérienne (on dit qu'ils sont bactériostatiques), ou tuent les bactéries (bactéricides).
Les figures 3 et 4 montrent quelques antibactériens importants. On pense souvent que la pénicilline est le premier antibactérien connu. En fait, très tôt, certains composés étaient utilisés contre les infections : eau de Javel(x) comme désinfectant [3], mercure contre la syphilis ; dès 1897, le médecin militaire Ernest Duchesne a traité avec succès des porcs atteints de typhoïde porcine par la moisissure Penicillium glaucum(xi). En 1911, avec le chimiste Alfred Bertheim et le bactériologiste Sahachiro Hata, Paul Ehrlich met au point le Salvarsan, actif contre la syphilis. En 1936, à l'Institut Pasteur de Paris, Thérèse et Jacques Tréfouël [4] synthétisent les sulfamides (fig 2), actifs contre de nombreux germes. Quant à la pénicilline, découverte par sérendipité [5] en 1928 par Fleming, son intérêt thérapeutique n'apparut que vers 1939(xii).
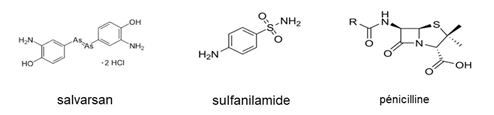
Figure 3. Antibactériens découverts par sérendipité
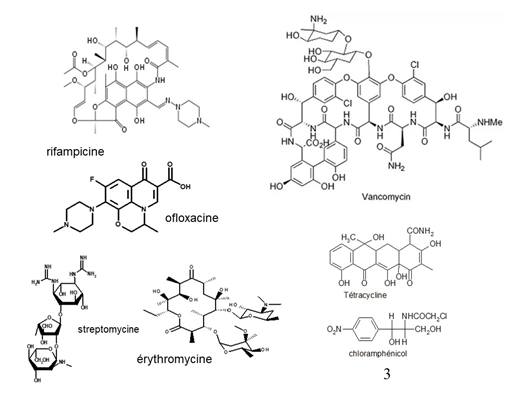
Figure 4. Exemples d’antibactériens
Le tableau 1 montre les dates d'apparition des principaux antibactériens, et leur origine. La plupart sont d'origine naturelle, mais des dérivés sont ensuite préparés par synthèse totale ou par hémisynthèse(xiii).
Pour combattre une infection, un antibactérien doit :
- entrer dans la bactérie et ne pas en être expulsé ;
- échapper à des mécanismes d'inactivation (enzymes) ;
- atteindre sa cible et la perturber en causant un dommage à la bactérie.
Cibles des antibactériens
Selon l'antibactérien, ce sont différents processus indispensables à la vie d'une bactérie que les antibactériens peuvent inhiber :
- Inhibition de la synthèse du peptidoglycane : la bactérie ne pourra plus fabriquer son enveloppe
- β lactames (pénicilline) et glycopeptides (vancomycine) ;
- Inhibition de la synthèse des acides nucléiques : la bactérie ne peut plus se multiplier
- ARN : rifampicine,
- ADN : quinolones (ofloxacine).
- Inhibition de la synthèse des protéines : la bactérie ne fabrique plus de protéines ou en produit de défectueuses. Elle n'aura plus les enzymes nécessaires à son métabolisme, par exemple :
- aminoglycosides (streptomycine),
- macrolides (érythromycine),
- tétracyclines,
- chloramphénicol.
En conclusion, même si nous disposons comme on le voit, d'un important arsenal chimique [6] pour lutter contre les maladies et en particulier les infections, la bataille est cependant difficile, des maladies comme la tuberculose, que l'on pensait quasiment éradiquée, continuent à exister, même dans les pays développés. Et il faut en plus compter avec la résistance que les bactéries peuvent développer. Sur ce sujet, consultez le Zoom sur la résistance des bactéries aux antibactériens.
Tableau 1 : Apparition de quelques antibactériens
| Classe | Date de la découverte → date d'élucidation de la structure | Origine |
| β-lactames: pénicillines | 1929 → 1945 | F |
| Sulfonamides | 1936 | S |
| Aminoglycosides | 1944 → 1947 | F |
| Phénicolés (chloramphénicol | 1948 → 1949 | F S |
| Peptides | 1948 → 1964 | F |
| β-lactames: céphalosporines | 1948 → 1961 | F |
| Macrolides | 1952 → 1965 | F |
| Tétracyclines | 1953 → 1962 | F |
| Streptogramines | 1955 → 1966 | F |
| Nitro imidazoles | 1960 | S |
| Rifampicine | 1960 → 1973 | F |
| Lincosamides | 1962 → 1964 | F |
| Acide fusidique | 1962 → 1965 | F |
| Quinolones | 1962 | S |
| Triméthoprime | 1962 | S |
| Glycopeptides | 1962 → 1983 | F |
| Fosfomycine | 1969 → 1969 | F S |
| Inhibiteurs de β-lactamases | 1975 → 1976 | F S |
| β-lactames: carbapénèmes | 1976 → 1978 | F S |
| Monobactames | 1979 → 1981 | F S |
F: obtenu par fermentation (produit naturel)
S: obtenu par synthèse
.jpg)
E. coli
(i) Pression qui détermine le phénomène d'osmose et qui correspond à la différence de pressions exercées de part et d'autre d'une membrane semi-perméable par deux liquides de concentration différente.
(ii) Les premiers hommes il y a seulement 10 millions d'années.
(iii) Hans Gram est un bactériologiste danois de la seconde moitié du XIXe siècle, qui a mis au point une coloration permettant de distinguer grâce à leur membrane deux types de bactéries : celles à Gram positif (Gram +) se colorent en rose, celles à Gram négatif (Gram -) ne se colorent pas.
(iv) Par exemple sur un doigt.
(v) Tout le membre.
(vi) Diffusée à tout l'organisme à partir du foyer initial : très grave.
(vii) Survenant à l'extérieur d'un établissement de santé.
(viii) Qui n'existaient pas chez le malade à son entrée à l'hôpital.
(ix) Lors d'une infection urinaire, on recommande de boire beaucoup : ainsi, si les germes infectieux sont peu adhérents, ils seront facilement éliminés.
(x) Hypochlorite de sodium, dont la découverte est attribuée à Claude Louis Berthollet en 1775, dans son usine du quartier de Javel à Paris.
(xi) Il a publié ce résultat sans savoir quelle substance était produite par son Penicillium.
(xii) On reverra avec intérêt le film « Le troisième homme ».
(xii) En partant de la molécule naturelle ou d'un précurseur.
Pour en savoir plus
[1] Parasite, champignon, bactérie et virus : quelles différences ?, N. J. Moreau, Question du mois, Mediachimie.org (2020)
[2] On regardera avec profit et plaisir la vidéo Bactéries, nos amies ? CERIMES (1 janvier 1990) Canal-u.tv
[3] Pourquoi ne pas mélanger de l’eau de Javel et du détartrant ?, F. Brénon,Question du mois, Mediachimie.org (2022)
[4] Thérèse et Jacques Tréfouël, le binôme indissociable, Institut Pasteur - Notre histoire
[5a] Il était une fois la sérendipité, S. Allemand et S. Catellin, Le Media Paris-Saclay (2014)
[5b] La sérendipité, un chemin de traverse à suivre, C. Monneret L'Actualité Chimique n°385 (mai 2014)
[6] Chimie et médicaments : un bel avenir !, B. Meunier, Colloque chimie et nouvelles thérapies (novembre 2019)
Crédits :
- illustration E. coli : Image par Gerd Altmann / Pixabay
- figures : © NJ Moreau
L’éclairage participe à près de 20 % de la consommation mondiale d’électricité. L’ADEME prévoit une baisse d’environ 50 % de la consommation liée à l’éclairage vers 2030 [1].
Par ailleurs, l’arrêt des ventes des lampes à incandescence d’une part, des lampes et tubes fluorescents et lampes halogènes d’autre part est fixé pour 2023. La période des fêtes de Noël voit chaque année les rues et places de nos villes et villages s’illuminer. L’éclairage est assuré par des diodes électroluminescentes pour diminuer les dépenses dues à la consommation électrique associée.
Une diode électroluminescente (DEL en français ou LED pour Light-Emitting Diode) est un dispositif électronique et optique produisant, sous l’action d’un champ électrique, de la lumière, sans créer de la chaleur contrairement aux lampes à incandescence. Pour qu’il y ait émission de lumière, l’utilisation de semiconducteurs est nécessaire. L’objectif est d’améliorer la conversion de l’énergie électrique en énergie lumineuse. La couleur dépend de la nature chimique du semiconducteur [2a] [2b].
Les premiers résultats de production de lumière rouge ont été obtenus dès 1962 par la General Electric. Les LED ont été utilisées sur des appareils électriques pour indiquer s’ils étaient allumés ou éteints. Mais les puissances étaient très faibles [3].
Ce n’est que dans les années 90 que l’utilisation du nitrure de Gallium (alliage GaN) comme semiconducteur a permis d’obtenir des LED avec en particulier une émission de lumière bleue difficile à obtenir mais essentielle par le mélange des couleurs pour créer la lumière blanche. Cette découverte a permis aux trois chercheurs japonais Isamu Akasaki, Hiroshi Amano et Shi Nakurama de recevoir le Prix Nobel de Physique en 2014 [3]. Les LED éclairent avec une puissance de 1 watt maximum pour un éclairage de 130 lumens bien supérieur aux tubes fluorescents (100 lumens par watt) [4].
Depuis, l’optoélectronique s’est tournée vers les diodes organiques électroluminescentes (OLED en anglais pour Organic Light Emitting Diode). Les OLED utilisent des semiconducteurs organiques. Elles possèdent de nombreux avantages : leur consommation est plus faible que celle des LED classiques et peuvent être fabriquées sur des supports souples permettant notamment leur enroulage (utilisés pour éclairer des décors ou des chantiers de construction par exemple). Elles sont utilisées principalement pour l’affichage électronique : smartphones, tablettes, téléviseurs [5].
Elles sont constituées d’une superposition de couches de matériaux organiques semiconducteurs constitués de polymères insaturés conjugués (c’est-à-dire avec alternance de liaisons simples et doubles dans leurs structures moléculaires) dans laquelle se trouve la couche émissive de lumière (EML pour Emissive Layer). Ces couches sont déposées entre deux électrodes : la cathode est souvent en aluminium et l’anode en oxyde d’indium et d’étain (ITO pour indium tin oxide) qui est déposée sur une couche transparente de verre par exemple. Les charges positives à la cathode et négatives à l’anode se déplacent sous l’action du champ électrique appliqué et se recombinent avec émission de lumière par fluorescence ou depuis 1998 par phosphorescence [6-8].
Si le système multicouche donne de bons rendements le dispositif reste complexe et les fabrications des OLED sont énergivores. Aussi de nombreux travaux de recherche ont été effectués pour obtenir des systèmes monocouches (SL pour Single Layer en anglais) conduisant à des SL-OLED. Récemment des travaux publiés en septembre 2022 par une équipe de recherche du CNRS menée par Cyril Poriel (Directeur de Recherche CNRS) basée à l’Institut des Sciences Chimiques de Rennes ont permis d’obtenir une SL-PhOLED (Ph pour phosphorescence) très efficace (la plus efficace à ce jour !). La couche émissive est ici constituée d’une matrice hôte et d’un émetteur phosphorescent. La matrice joue un rôle primordial et permet de maximiser l’efficacité de l’émission de lumière. Elle est constituée d’une partie riche en électrons et d’une seconde pauvre en électrons reliées entre elles par une structure non plane de type spirannique (les spirannes sont en effet des molécules bien connues au sein du laboratoire rennais !) qui permet une séparation spatiale des charges pour réunir les propriétés souhaitée (figure 1).
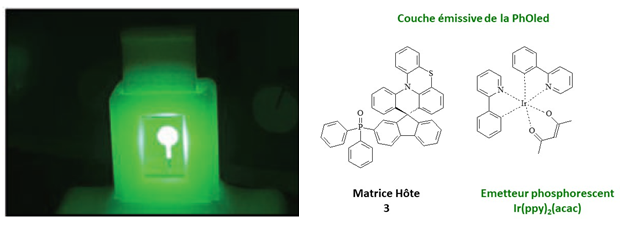
Figure 1. SL-PhOLED verte utilisant la couche émissive la plus performante de la littérature (2022, EQE > 22 %)
Source : photo reproduite avec autorisation de Lucas. F., Brouillac. C., Fall. S., Zimmerman. N., Tondelier. D., Geffroy. B., Leclerc. N., Heiser T., Lebreton. C., Jacques. E., Quinton. C., Rault-Berthelot. J., Poriel C., Chem. Mater. 2022, 34, 8345 copyright 2022 American Chemical Society.
Pour augmenter l’efficacité de l’émission de lumière un émetteur phosphorescent est nécessaire, par exemple un complexe d’iridium pour une émission de lumière verte (voir note) avec une efficacité supérieure à celles obtenues antérieurement [9]. L’objectif ultime est de développer des SL-PhOLED à émission de lumière blanche pour l’éclairage !
La simplification électronique obtenue avec les SL-PhOLED permet un développement prometteur de cette technologie qui s’accompagne aussi d’une production moindre de déchets !
L’auteur remercie très sincèrement Cyril Poriel, pour son aide bienveillante à la rédaction de cette note bibliographique et son autorisation de publier la photo de la diode verte et des structures de la couche émissive (voir la note).
Jean-Pierre Foulon
Mars 2023
Références bibliographiques :
[1] Rapport ADEME 2016
[2a] EnLEDissez-vous !, J.C. Bernier, L’Actualité Chimique N°395 (avril 2015) pp. 9-10
[2b] La lumière électronique : du tube cathodique aux écrans plats, J.C. Bernier, Colloque Chimie et Lumière du 26 février 2020, vidéo et article (Mediachimie.org)
[3] De la lampe à huile aux LED : histoire physico-chimique de l’éclairage artificiel, L. Simonot, Colloque Chimie et Lumière du 26 février 2020, vidéo et article (Mediachimie.org)
[4] Un prix Nobel éclairé, J.C. Bernier, éditorial Mediachimie (octobre 2014)
[5] Chimie, lumière sur les écrans, J. Lefebvre, A. Harari et J.-C. Bernier, fiche Chimie et… en fiches (Mediachimie.org)
[6] Les diodes électroluminescentes organiques : des sources plates de lumière, L. Hirsch, Colloque Chimie et technologies de l’information du 6 novembre 2013, vidéo et article (Mediachimie.org)
[7] Les multiples contributions de la chimie dans la conception des tablettes et des smartphones, J.-C. Flores, Colloque Chimie et technologies de l’information du 6 novembre 2013, vidéo et article (Mediachimie.org)
[8] Un point sur Les nouvelles générations d’OLED phosphorescentes, C. Poriel, L’Actualité Chimique N°454 (septembre 2020) p. 75
[9] Un point Les OLED à couche unique : vers des dispositifs électroniques simplifiés pour la transition écologique, C. Poriel, L’Actualité Chimique N°481 (février 2023) p. 55
Crédits : La SL-PhOLED verte : photo reproduite avec autorisation de Lucas. F., Brouillac. C., Fall. S., Zimmerman. N., Tondelier. D., Geffroy. B., Leclerc. N., Heiser T., Lebreton. C., Jacques. E., Quinton. C., Rault-Berthelot. J., Poriel C., Chem. Mater. 2022, 34, 8345 copyright 2022 American Chemical Society.
Lorsqu’en 1774 paraît le premier tome des Voyages métallurgiques entre 1757 et 1769, son auteur Antoine Gabriel Jars, dit le Jeune, est mort depuis 1769. C’est son frère ainé Gabriel Jars (1729-1808) dit l’Ancien, qui fait imprimer l’ouvrage en trois tomes, les deux derniers tomes seront publiés jusqu‘en 1781. Le premier tome est consacré à la houille et au fer, les deux autres à la métallurgie non-ferreuse. L’ensemble est constitué de mémoires.
Gabriel Jars le Jeune est né en 1732 à Lyon. Son père est Directeur des mines et Jars le Jeune s’intéresse très tôt à la métallurgie. Remarqué par ses professeurs, il entre à l’École royale des Ponts et Chaussées à Paris en 1752 dans une classe spéciale réservée aux mines. Cette école fondée en 1747 par Daniel Charles Trudaine (1703-1769), a pour mission de former les techniciens et les ingénieurs. Trudaine comme Jean Hellot (1685-1766) veut faire avancer le bien-être de la société grâce au progrès technique par l’éducation, la formation et l’apprentissage. Le jeune Gabriel est envoyé en stage dans les mines de plomb argentifères de Poullaouen en Bretagne. Puis sur d’autres sites comme les mines d’argent de Sainte-Marie aux Mines en Alsace.
Ses études terminées, il revient dans l’exploitation familiale où il met en œuvre un four à réverbère où la chaleur du four est réfléchie par la voute du four, ainsi qu’un four à cuivre.
Grand ingénieur d’Etat, sa réputation lui vaut dans les années 1750-1760 de devenir membre correspondant de l’Académie royale des Sciences de Paris en 1761 puis d’être élu, simultanément à Antoine Laurent Lavoisier (1743-1794), au fauteuil de chimie laissé vacant en 1768 par le Théodore Baron d’Hénouville (1715-1768). Gabriel Jars est ainsi récompensé pour son apport.
Gabriel Jars voyage dans une grande partie de l'Europe Centrale et en Grande-Bretagne, afin de rapporter en France le meilleur des pratiques techniques qu’il croise et relève en chemin. Trois années durant, de 1757 à 1760, accompagné de Jean-Pierre-François Guillot-Duhamel (1730-1816), il visite des mines et des fonderies dans de nombreuses régions : Saxe, Autriche, Bohême, Hongrie, Tyrol, Carinthie et Styrie. Puis, de nouveau à la demande du gouvernement, il part l’année 1765 complète en Angleterre. À peine revenu en France, il repart vers les pays du nord en compagnie de son frère. Ils commencent leur périple par la Hollande et ses manufactures, puis le Hanovre, séjournent quatre mois dans les montagnes du Harz, parcourent une partie de la Saxe puis se rendent à Hambourg, de là à Copenhague, puis aux mines d'argent de Kongsberg en Norvège et enfin en Suède.
Ensuite, il réalise des missions en France afin d’étudier les mines près de Langeac, actuellement en Haute-Loire. Mais la forte chaleur le rend malade et il est ramené à Clermont-Ferrand où il meurt d’insolation le 20 août 1769.
Il a passé l’essentiel de sa vie à voyager à travers l’Europe et à observer les techniques employées dans les forges, pour les introduire sur le territoire français, avec le souci permanent de lier théorie et pratique. Son journal de voyage permet de recueillir des informations au jour le jour et ce travail devient au XIXe siècle, l’exercice obligé de tous les élèves ingénieurs des Écoles des Mines de Paris comme de Saint-Étienne.
Gabriel Jars le Jeune est un métallurgiste, créateur de la sidérurgie française et aussi un innovateur en introduisant des nouveaux procédés. On lui doit la fonte au coke ; le procédé de fabrication du minium, qu’il présente à l’Académie des Sciences en avril 1768. Pour lui, le charbon et le fer sont les éléments essentiels du développement technique. Enfin, il installe au Creusot un grand centre industriel qui existe toujours.
Son ami, Jean-Pierre-François Guillot-Duhamel continuera l’œuvre de Gabriel Jars en introduisant des procédés nouveaux comme la cémentation de l’acier. Il collaborera à l’Encyclopédie méthodique d’Antoine-François Fourcroy (1755-1809) en rédigeant les articles concernant les mines et la métallurgie.
Pour en savoir plus
- La famille Jars et sa contribution à l'exploitation des mines lyonnaises au XVIIIe et au XIXe siècles, Alexis Chermette, Publications de la Société Linnéenne de Lyon (1981) Vol 50-5 pp. 1-11
- Jars Le voyageur innovant Anne-Françoise Garçon (2000) ⟨halshs-00008092⟩
- Les Voyages métallurgiques de Gabriel Jars (1774-1781), un imprimé au service de l’art de l’exploitation des Mines, Isabelle Laboulais, in Les circulations internationales en Europe (1680-1780), Presses Universitaires de Rennes (2010) pp.181-196
