À J -125, la tenue des 45 000 volontaires des Jeux Olympiques et Paralympiques élaborée par Décathlon a été dévoilée. Ces tenues, puisque plusieurs pièces (chaussures, chaussette, pantalon double fonction, tee-shirts, chapeau, banane, marinière transformable, chapeau, sac) constituent ce bagage vestimentaire, ont été testées par les athlètes et élaborées par le fabricant en répondant aux critères suivants : déperlance, élasticité, résistance, ergonomie.
Cet uniforme des volontaires fortement identifiable allie fonctionnalité et confort. Il est annoncé comme éco-conçu, moderne et modulable. Dans une volonté d’éco-conception et d’éco-responsabilité, l’ensemble de cette panoplie, unisexe, a été réalisée avec une part importante de Made in France.
La chimie, une fois de plus, a œuvré pour proposer des textiles adaptés aux volontaires. Si dans ce cas la quête de performances sportives n’est pas de mise, il n’empêche que les textiles proposés répondent en tous points à ceux des sportifs de haut niveau et donc aux contraintes de température extérieure, de température du corps et aux critères fixés ci-dessus par le COJO.
Pour en savoir plus sur le sujet consultez nos articles :
- Des textiles pour sportifs. Apport de la chimie pour améliorer confort et performances
- La chimie dans le sport : chimie et matériaux
- Combinaisons en néoprène® calcaire ou en néoprène® aux coquilles d’huîtres : renouvelables ou non ? (Question du Mois)
- Sport et chimie (liste de ressources)
Alors ouvrons grands les jeux !
Jean Gomez
Crédit illustration : © Paris 2024 x Decathlon
La semaine de la presse et des médias à l’école nous donne l'occasion de nous poser la question des sources de ces flux d'informations qui nous arrivent en continu. L'information est nécessaire pour comprendre le monde, mais elle est aussi porteuse du pire : désinformation, information bousculée ou détournée par l'intelligence artificielle…
La chimie est souvent prise pour cible et sujette à des informations erronées. Nous vous proposons donc d’aborder une question pour laquelle nos experts ont analysé les informations disponibles dans les médias et apportent un éclairage scientifique critique :
- Les combinaisons en néoprène® calcaire ou en néoprène® aux coquilles d'huîtres : renouvelables ou non ?
Pour aborder en classe ce sujet, les élèves de niveau premières et terminales scientifiques et technologiques peuvent lire les deux articles suivants :
- Des combinaisons marines fabriquées avec des coquilles d’huîtres, Ouest France (02/06/2021)
- A La Rochelle, une combinaison de surf fabriquée à base de coquilles d’huîtres, Le Parisien (01/02/2020)
puis décrypter ces informations avec par exemple deux questions :
- Est-il vraiment possible de faire une combinaison de plongée avec des coquilles d'huitres ?
- Est-ce écologiquement vertueux comme supposé dans les articles ?
Pour vous aider à y voir plus clair, consultez la Question du mois : Combinaisons en néoprène® calcaire ou en néoprène® aux coquilles d’huîtres : renouvelables ou non ?
Vous pratiquez la plongée sous-marine, le surf ou autres sports nautiques et vous utilisez des combinaisons isothermes en « néoprène® ». Au moment d’acheter votre combinaison vous vous posez la question : laquelle choisir qui soit à la fois performante et respectueuse de l’environnement ? Une recherche sur Internet avec le mot-clef « néoprène » vous propose des alternatives écologiques à leur fabrication.
Voici quelques propositions trouvées et reprises de très nombreuses fois sur Internet par les services commerciaux de vendeurs de combinaisons.
- Nos combinaisons sont en « néoprène issu du calcaire contrairement à la plupart des néoprènes issus de produits pétrochimiques. »
- « Le néoprène biologique Yamamoto est respectueux de l’environnement et se compose à 99.7% de carbonate de calcium »
On notera que sur le site de Yamamoto (i) il est écrit : YAMAMOTO est fier d'utiliser Limestone CR à 100 %. Le calcaire est fabriqué à partir du mont Kurohime qui stocke des milliards de tonnes de calcaire le plus pur. A partir de ce calcaire le plus pur, YAMAMOTO utilise uniquement le calcaire de la plus haute qualité, contenant 99,7 % de carbonate de calcium… Le pourcentage de 99,7% ne concerne donc pas le néoprène. - Un numéro de mars 2021 du magazine de l’ADEME (ii), a pour titre « Des combinaisons de surf à base de coquilles d’huîtres ». Il y est précisé : « Le dernier modèle conçu par l’entreprise est fabriqué à partir de coquilles d’huître broyées. Une matière 100 % naturelle et renouvelable qui remplace le limestone que l’on trouve dans la composition du néoprène des combinaisons classiques ». Cette information a été également reprise par la presse (iii).
Alors décryptons tous ces mots et posons-nous la question : comment peut-on fabriquer une combinaison en néoprène® à partir de pétrole ou à partir de calcaire et celle-ci est-elle une alternative écologique ?
Tout d’abord qu’est-ce que le néoprène® ? [1] [2]
C’est un nom commercial (iv) devenu un nom courant pour désigner le caoutchouc de polychloroprène (noté souvent par le sigle CR pour Chloroprène Rubber). Il n’existe pas dans la nature (v), c’est donc un produit de synthèse.
Il faut disposer d’une molécule monomère, le chloroprène (vi), qui pourra réagir sur elle-même un très grand nombre de fois pour former de très longues chaines moléculaires où les atomes de carbone s’enchainent, pour conduire au polymère, le polychloroprène (cf. figure1).
(n peut être de plusieurs milliers) | |
Figure 1
Il faut donc tout d’abord créer le chloroprène.
Il existe 2 voies de synthèse : soit à partir du pétrole (de très loin la plus répandue depuis 1960) soit à partir d’un mélange de calcaire et de charbon [1] [2] [3] [4].
La première voie passe par l’obtention de butadiène molécule obtenue en très grande quantité (vii) au cours du vapocraquage des essences légères issues du pétrole (viii)(ix).
La deuxième voie passe par l’obtention d’acétylène à partir de calcaire ou limestone (x) et de charbon. Le calcaire est du carbonate de calcium CaCO3 et le charbon est la source de carbone C.
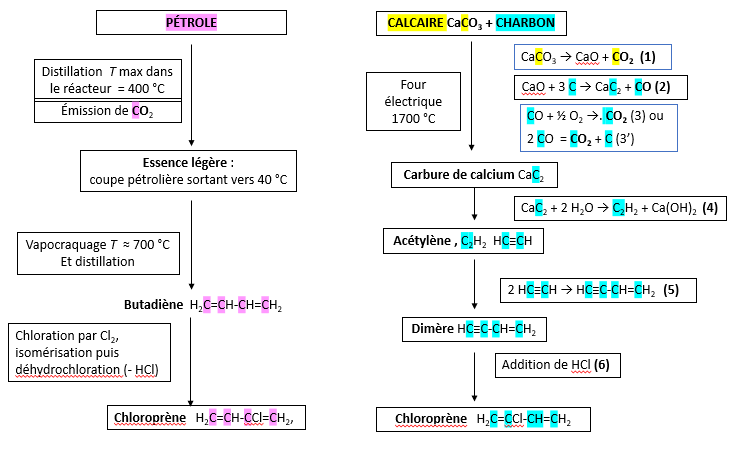
Tableau comparatif des 2 voies par Françoise Brénon
Les atomes de carbone surlignés en jaune (C) proviennent du carbonate de calcium, ceux surlignés en turquoise (C) proviennent du charbon et ceux surlignés en rose (C) proviennent du pétrole. Mais bien sûr, la molécule de chloroprène qu’elle soit dérivée du pétrole ou du calcaire est chimiquement unique. Les atomes de carbone n’ont pas de mémoire !
Et observons que le carbone contenu initialement dans le calcaire se trouve dans CO2 formé (réaction 1).
Alors cette deuxième voie est-elle plus respectueuse de l’environnement ?
Certes elle n’utilise pas de pétrole, ressource non-renouvelable. Mais les mines de calcaire non plus ne sont pas renouvelables et surtout les atomes de carbone provenant du carbonate de calcium se trouvent dans CO2 dégagé ! Au total, pour cette voie, le dioxyde de carbone formé provient pour moitié du carbonate, CO2, cf. réaction (1) et pour l’autre moitié du charbon CO2, cf. réactions (3 et 3’).
Enfin ce procédé très énergivore soulève la question de l’énergie électrique utilisée : est-elle verte et renouvelable, ou non ?
Peut-on dire que « le néoprène calcaire se compose à 99.7% de carbonate de calcium ? »
Cette phrase qui apparait dans de nombreuses communications commerciales n’a pas de sens : elle laisserait à penser que la combinaison est essentiellement constituée de calcaire pratiquement pur ce qui est absurde ou que les atomes de carbone du polychloroprène sont ceux issus du carbonate CaCO3, ce qui est faux.
En effet, pour que le carbonate de calcium soit considéré comme la matière première durable de la fabrication du néoprène, il aurait fallu que l’atome de carbone contenu dans CaCO3 soit la source des atomes de carbone qui constituent la chaine polymérique du néoprène. Or il n’en est rien : le carbone présent dans la chaine du néoprène -(CH2-CCl=CH-CH2)n- provient exclusivement du charbon. On devrait plutôt l’appeler le néoprène charbon !
Remplacer le calcaire des mines par des coquilles d’huîtres : quelle conséquence ? Cela rend effectivement le carbonate de calcium renouvelable, mais cela s’accompagne toujours du même dégagement de CO2 et ne change pas la source des atomes de carbone du chloroprène.
Quant à l’obtention de carbone, nécessaire à la réaction (2) issue de coke, elle est très polluante. Celle à partir de charbon de bois l’est moins et est biosourcée, mais peut être source de déforestation.
Le néoprène limestone est-il biologique ?
Le terme biologique signifie « Qui a rapport à la vie, aux organismes vivants ». Alors, affirmer que le néoprène calcaire ou limestone issu de mines est un néoprène biologique traduit ici une utilisation inappropriée voire trompeuse du terme biologique !
C’est la double utilisation de la coquille d’huître et de carbone biosourcé, ce qui n’est pas cité dans les articles, qui permettrait de donner à cette fabrication un caractère renouvelable (tout en restant très énergivore et en libérant du CO2).
Comment passe-t-on aux mousses néoprène ?
C’est en réalité ces étapes qui vont différencier les qualités des mousses dont sont faites les combinaisons.
Tout d’abord le chloroprène est polymérisé en polychloroprène (xi). Il existe plusieurs grades et viscosités de polychloroprènes. Il est à noter que le chloroprène est fabriqué seulement pour la synthèse du polychloroprène et qu’il existe peu de producteurs dans le monde (xii).
Les fabricants de mousse achètent le polychloroprène aux producteurs précédents. Pour réaliser la mousse, ce polymère est mélangé avec une huile qui sert de liant, des charges renforçantes comme le noir de carbone (xiii), des réactifs pour mener à bien la vulcanisation (xiv), c’est-à-dire créer des ponts entre les différentes chaines de polychloroprène, et divers additifs (xv) dont un générant des bulles de gaz in situ, pour conduire à des mousses alvéolées vendues sous formes de feuilles de différentes épaisseurs.
Le noir de carbone peut provenir de pneus recyclés qui vont subir d’abord une pyrolyse (xvi) [5].
Les procédés mis en jeu peuvent fortement varier d’un fabricant (xvii) à l’autre et vont conduire à des mousses néoprène de différentes qualités.
Et la combinaison ?
Le fabricant de combinaisons achète et sélectionne la qualité et l’épaisseur des feuilles de mousse de néoprène et les associe à des tissus extensibles (xviii) en plusieurs couches contre collées. Les étapes finales sont du ressort de la confection. La qualité des coutures, assemblage cousu-collé est importante pour l’étanchéité.
Alors quelle alternative au pétrole ou au charbon pour une combinaison néoprène ?
Utiliser par exemple des déchets ou résidus agricoles constituant une biomasse pour obtenir un butadiène biosourcé [6].
Les sociétés Michelin, IFPEN et Axens sont très impliquées dans cette approche à partir d’éthanol issu de cette biomasse et démarrent une unité expérimentale en France en 2024 (xix). Ce procédé présente globalement une très faible émission de gaz à effet de serre. Le chloroprène obtenu à partir de ce butadiène biosourcé serait une piste plus écologique.
Et dans une approche d’économie circulaire il faut récupérer les combinaisons usagées. Actuellement des filières se mettent en place. Pour le moment, certaines combinaisons sont broyées mais le résidu est utilisé dans d’autres applications (xx).
Remarque : il existe d’autres combinaisons pour les sports nautiques utilisant par exemple du caoutchouc naturel (naturel rubber NR) ou des mélanges. Elles ne doivent pas porter le nom de néoprène synonyme de polychloroprène. Certains noms commerciaux ambigus sont aussi des sources de confusion.
Conclusion
Il ne faut pas se laisser tromper par les termes chocs utilisés à mauvais escient sans prise en compte de la réalité scientifique comme argument de vente mais il faut développer son esprit critique. Afin de prouver techniquement et scientifiquement que l’option retenue puisse être déclarée « plus respectueuse de l’environnement », il est nécessaire de réaliser l’analyse du cycle de vie du produit fini intégrant toutes les étapes de fabrication et elle doit prendre en compte une multitude de critères selon les principes de la chimie verte [7].
Par exemple tenir compte ici :
- du bilan énergétique global selon les deux voies, sans oublier l’extraction du calcaire ou le ramassage des coquilles et du transport à l’usine pour la voie acétylène ;
- du type de source de carbone dans le cas de la voie acétylène à comparer à la source pétrole ;
- des émissions de dioxyde de carbone et leurs éventuelles compensations lors de l’usage de réactifs biosourcés.
Françoise Brénon et Gérard Roussel
Ajout mai 2024 : vous pouvez également regarder cette vidéo de « Blablareau au labo » sur le sujet.
(i) https://yamamoto-bio.com/material-e/sus2.html
(ii) Des combinaisons de surf à base de coquilles d’huître, ADEME Magazine (mars 2021) ADEME, Agence de la transition écologique.
(iii) Par exemple dans Ouest France sous le titre « Des combinaisons marines fabriquées avec des coquilles d’huîtres » (publié le 2/06/2021) et dans Le Parisien avec le titre « A La Rochelle, une combinaison de surf fabriquée à base de coquilles d’huîtres » (publié le 1/02/2020)
(iv )Néoprène est un nom de marque de la compagnie américaine Dupont, donné dès 1930, à son produit à base de polychloroprène.
(v) Contrairement au caoutchouc naturel, (NR, pour Natural Rubber), obtenu à partir de la sève de l’hévéa.
(vi) En nomenclature il s’appelle le 2-chlorobuta-1,3-diène
(vii) Le butadiène est aussi très utilisé pour l’obtention d’autres caoutchoucs synthétiques et 40 % de sa production est consommée par les pneumatiques.
(viii) Raffinage pétrolier, fiche pédagogique sur le site Connaissancedesenergies.org
(ix) Vapocraquage = cassures de molécules en présence de vapeur d’eau, pour obtenir des molécules de longueur plus courtes. La température est voisine de 700 °C et varie selon la composition de l’essence légère dont on part. https://lelementarium.fr/focus/vapocraquage-des-hydrocarbures/ et https://fr.wikipedia.org/wiki/Vapocraquage
(x) Limestone est le mot anglais pour calcaire.
(xi) Exemples de grades de polychloroprène société DENKA (Japon)
(xii) Les fabricants de chloroprène et de polychloroprène sont, en 2024, Asahi Kasei (Japon), BRP Manufacturing (USA), Canada Rubber Group, Chongqing Changshou Chemical (Chine), Denka (Japon) qui a repris l’activité de Dupont de Nemours aux USA en 2014 et produit le CR aux USA à partir du butadiène, et au Japon à partir du calcaire et du charbon (voir page 9 et 10 de General Introduction and Some Advances on Denka Neoprene® Latex (PDF)), ARLENXEAO (Pays-Bas / France), Macro International (USA), SHOWA DENKO K.K. (Japon), Tosoh (Japon) et Zenith Industrial Rubber Products (Inde).
Sources : https://www.researchandmarkets.com/reports/5143078/global-neoprene-market-2020-2024?w=4 et https://www.usinenouvelle.com/article/arlanxeo-totalement-aux-mains-de-saudi-aramco.N1240402
(xiii) L’ajout de noir de carbone donne la couleur noire aux combinaisons. Mais c’est surtout un excellent agent de protection contre les UV et l’abrasion et il apporte une ténacité à la mousse caoutchoutique. Il peut représenter 30 % de la mousse.
(xiv) Le système de vulcanisation contient de l’oxyde de zinc ZnO, de l’acide stéarique, du soufre ou produits soufrés et des accélérateurs de vulcanisation.
(xv) Parmi ces additifs on trouve des antioxygène, anti-ozone, ignifugeant et des composés générant un gaz (azote en général).
(xvi) La pyrolyse des pneus, préalablement broyés, consiste en une décomposition chimique par une très forte augmentation de température en l'absence d'oxygène, pour conduire à du carbone.
(xvii) Le leader mondial du marché dans la production de mousse néoprène pour combinaison est la société SHEICO basée à Taïwan et qui a ses usines dans l’Asie du Sud-Est.
(xviii) Fibres synthétiques telles que le polyester ou l’élasthanne dérivé du polyuréthane.
(xix) Inauguration d’un démonstrateur en janvier 2024. Voir https://www.ifpenergiesnouvelles.fr/article/inauguration-du-1er-demonstrateur-industriel-francais-production-butadiene-partir-dethanol-biosource et le schéma réactionnel sur le site de l’IFPEN.
(xx) https://surfwear.sooruz.com/webshop/fr/153-recyclage-combinaison-surf
Pour en savoir plus
[1] Le néoprène, L. Dollinger et P. Ledesma-Diaz-Caneja (2017) sur le site Ramène ta science (Chimie Paris ParisTech PSL)
[2] Manufacture and use of chloroprene monomer, M Lynch, Chemico-Biological Interactions, 135-136 (2001) pp. 155-167
[3] Chloroprène par la voie du pétrole sur le Portail Substances Chimiques de l’INERIS
https://substances.ineris.fr/fr/substance/getDocument/2557 (PDF)
[4] The footprint chronicles: green neoprene? (PDF) 2012 Patagonia
[5] Vidéo d’obtention de la mousse de néoprène (en anglais) par la société Sheico disponible sur YouTube
[6] Les chimistes dans : La chimie du végétal comme substitut du pétrole, F. Brénon et G. Roussel, Série Les Chimistes dans (Mediachimie.org)
[7] La chimie peut-elle se mettre au vert ?, Eric Bausson, Dossier pédagogique Éditions Nathan / Fondation de la Maison de la Chimie (Mediachimie.org)
Crédit illustration : Kate Baucherel / Pixabay, licence de contenu Pixabay
L’ouvrage Chimie et matériaux stratégiques est disponible en ligne en PDF.
Retrouvez tout le colloque en détail : les vidéos, les chapitres des conférences, les quiz…

La civilisation est née avec les matériaux ; elle risque maintenant de mourir si l’humanité ne sait plus les gérer. En effet, leurs usages ont complètement changé depuis les dernières décennies.
Citons les deux raisons majeures :
- Matériaux et rareté des matières premières, cela va ensemble, l’usage des métaux le montre depuis la préhistoire, la gestion des forêts aussi, origine de l’effondrement de grandes aventures humaines ! Et cette rareté nous guette car de mille côtés, les besoins de nouvelles technologies se développent pour la transition énergétique, pour le numérique... Rareté, cela signifie disparition possible et donc « catastrophes », d’où l’emploi du qualificatif « stratégique » pour ce colloque.
- Le réchauffement climatique, dont plus personne ne doute, impose des contraintes exceptionnelles sur les besoins en matériaux. Les énergies solaire ou éolienne, par exemple,réclament des métaux « rares » dont la pérennité n’est pas assurée. L’impératif de lutter contre l’émission du CO2 accroît considérablement les besoins de nouveaux matériaux (biosourcés par exemple), car les procédés de fabrication doivent être revus en profondeur et faire exploser les besoins en matériaux. Le recyclage doit être mis au point pour rendre tout cela compatible.
Des spécialistes des diverses disciplines appelés à la manoeuvre (minéralistes, polyméristes, biologistes, ingénieurs) se mobilisent dans cet ouvrage pour analyser cette complexité, qui est l’enjeu vital de notre époque. Ils mettent à la portée des étudiants et des chercheurs les points prioritaires de la recherche en chimie pour « matériaux stratégiques » devenue aujourd’hui vitale.
Commander le livre sous format papier.
Retrouvez les derniers colloques Chimie et… dans l’Espace Colloques.
Sitôt cueilli le raisin est pressé et donne un jus (le moût) dans une limite réglementaire : 4000 kg de raisins contenus dans un pressoir classique ne doivent pas fournir plus de 2550 L de moût. Ce dernier contient 18 % de « sucre » et doit contenir au minimum 7,5 % d’alcool pour l’appellation géographique protégée. L’alcool provient d’une réaction de fermentation naturelle. Pour obtenir un vin de champagne il faut augmenter le taux d’alcool. C’est pour cela qu’on ajoute au moût du sucre et des levures sélectionnées, actuellement commercialisées sous forme sèche. Le sucre ajouté est du saccharose (C12H24O12), à raison de 3,36 kg par hL de moût, qui s’hydrolyse en glucose et fructose, deux molécules isomères de formule C6H12O6. Ce moût additionné de sucre est fermentescible. […]
Accédez au Zoom sur Le CO2 dans une bouteille de champagne
Crédit illustration : Aprilante / iStock
Le 29 janvier dernier, le jury du GPJJC (Grand Prix des Jeunes Journalistes de la Chimie) s’est réuni à la Fondation pour sélectionner les 4 binômes qui allaient participer à l’édition 2024 du GPJJC.
Les 4 dossiers retenus sont les suivants.
- Comment les PHAs peuvent permettre à la France d’atteindre l’objectif zéro pollution plastique ?
Sarah Costes et Roméo Marmin – École publique de journalisme de Tours (EPJT) - Comment la mécanochimie veut-elle verdir la fabrication de nos médicaments ?
Candice Antiga et Taslime Maazouzi – Centre de formation des journalistes (CFJ) Paris - L’utilisation des nouvelles techniques d’imagerie chimiques pour étudier les peintures archéologiques
Caroline Barathon et Cléa Dubray – École de journalisme de Grenoble (EJDG) - Décarbonation du ciment, se passer du clinker pour diminuer les émissions de CO2
Morgane Anneix et Juliette Laffont – École de journalisme Sciences Po Paris
La prochaine étape sera la rencontre avec le jury le 12 mars prochain à la Fondation, puis trois mois d’investigations pour produire un article et une vidéo.
Nous souhaitons bonne chance aux 4 binômes qui vont concourir.
Rendez-vous en juin pour visionner et lire les productions et surtout connaître le binôme vainqueur du GPJJC 2024.
Les vidéos et résumés des conférences du colloque Chimie et sports en cette année Olympique et Paralympique du 7 février 2024 sont disponibles sur Mediachimie et sur Youtube ainsi que sur Viméo/Fondation de la Maison de la chimie.
Le quiz post-colloque est également en ligne. À vous de jouer !
Vous qui n’avez pas la possibilité de venir à la Fondation de la Maison de la Chimie le 7 février 2024, vous pouvez assister en direct au Colloque Chimie et Sports en cette année Olympique et Paralympique
sur Mediachimie ou sur Youtube
Vous pouvez aussi tester vos connaissances sur le sujet avec ce quiz.
Ajout du 10/02/2024 : Les résumés et vidéos sont disponibles sur Mediachimie ou sur Youtube ainsi que sur Viméo.
Le caramel aurait été inventé vers l'an 1000 par les arabes au cours de la manipulation du sirop de canne à sucre. Son nom, apparu au XVIIe siècle viendrait, via le portugais camelo, du latin Calamellus, diminutif de calamus, « roseau », à cause de l'analogie de forme entre le sucre durci et la tige de roseau (i).
Il ne faut pas confondre les caramels, friandises dures ou molles, contenant généralement du caramel et d'autres ingrédients (ii), et le caramel, c'est à dire la substance brune à l'odeur et au goût caractéristiques. Pour faire du caramel à la maison, on chauffe du sucre dans une casserole, éventuellement après l'avoir dissous dans un peu d'eau. Selon la durée de cuisson, on aura un caramel clair ou un caramel plus foncé.
Mais quel est donc que ce composé coloré et comment se forme-t-il ?
Les réactions
À la cuisine
Quand on chauffe la solution de sucre (ou le sucre en poudre seul), de l'eau s'évapore (la température est alors de 100°C) et le composé reste blanc. Si on continue, la température s'élève, et une couleur dorée ainsi que la bonne odeur caractéristique du caramel apparaissent vers 160°C. Si on continue à chauffer, la couleur s'intensifie et le caramel devient brun. Le stade « caramel blond » est difficile à saisir, car dès que la température de 160°C est atteinte, cela va très vite évoluer (iii)… Les industriels, pour faire des substances conférant le parfum caramel, ajoutent des produits qui vont ralentir cette évolution, comme de la crème, qui donnera des caramels mous, ou du beurre, du sel, du citron etc. (ii). Ces caramels modifiés seront alors considérés comme des additifs des friandises auxquelles ils sont ajoutés.
Que se passe-t-il ?
Si la glace fond lorsqu’on la chauffe, on la retrouve en refroidissant. C’est réversible. Pas pour le caramel.
C'est que la glace est un composé unique, H-O-H, alors que le sucre de table ou saccharose (iv), C12H22O11, est un disaccharide (v) formé de deux molécules, glucose (cycle à 6 atomes) et fructose (cycle à 5), chacune de formule C6H12O6 liées de façon très spécifique (fig. 1).
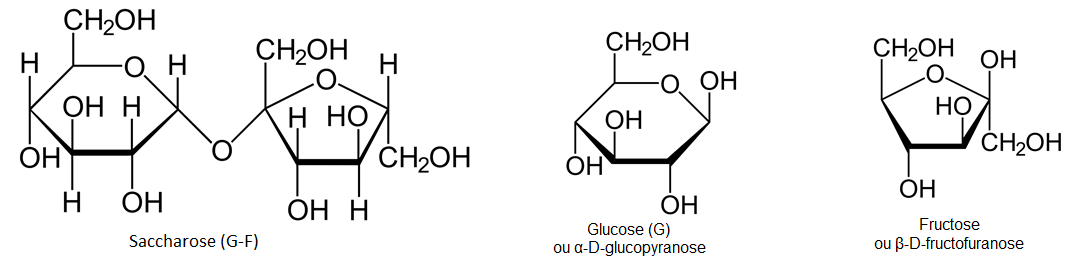
Figure 1 (vi). Formule du saccharose (G-F), du glucose (G) ou α-D-glucopyranose, du fructose (F) ou β-D-fructofuranose.
Lors du chauffage, ces deux molécules vont se séparer, et peuvent réagir l'une sur l'autre, soit comme initialement, G-F, soit F-G ou G-G ou F-F et cela en diverses positions. En outre, ces monoses sont fragiles, et comme on le verra plus loin, peuvent se modifier, ce qui complique encore les choses. En regardant les formules, avec toutes ces fonctions alcool, on comprend la difficulté de répondre à la question « qu'est-ce que le caramel ? ».
Il y a environ 200 ans Péligot [1] a fait la première publication sur le sujet, et ce n'est qu'en 1989 [2] que la fraction volatile du caramel, responsable de son odeur, a été identifiée comme le 5-(hydroxyméthyl)-2-furfuraldéhyde (fig. 2). Mais pendant longtemps, on a ignoré la nature exacte du caramel.
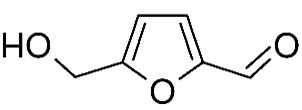
Figure 2 (vii). 5-(hydroxyméthyl)-2-furfuraldéhyde
Un peu plus de chimie et l'élucidation du mystère
Souvent, quand vous parlez de la chimie du caramel, on vous répond « Ah oui, bien sûr, la réaction de Maillard ! ». Ce n'est pas exact, cette dernière est caractéristique de la saveur des viandes grillées,
et nécessite la présence de protéines ou d'acides aminés [3]. Mais la caramélisation appartient, comme la réaction de Maillard, au groupe des réactions de brunissement non enzymatique des aliments. Un article de 2000 [4] élucide complètement le mystère.
Lorsqu'on chauffe la solution de saccharose, le disaccharide s'hydrolyse en glucose et fructose. Une catalyse acide facilite la réaction, d'où l'addition recommandée de jus de citron pour faire du caramel. Le fructose donne rapidement des dianhydrides de fructose (DAF) par dimérisation (fig. 3). On sait que les monoses, représentés sous forme cyclique, sont des acétals cycliques et qu'ils sont en équilibre avec la forme ouverte (fig. 4). C'est ce qui permet d'expliquer la formation des anhydrides. Mais il y a de multiples possibilités et plusieurs isomères en équilibre. Ces molécules se retrouvent à plus de 80% dans le caramel fait avec du fructose.
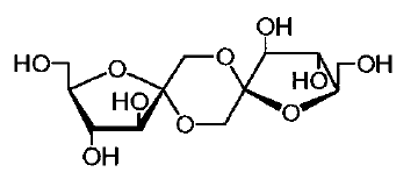
Figure 3. Exemple de dianhydride de fructose, DAF
Source : L'Actualité chimique (novembre 2000) p 25 (schéma 1) [4]
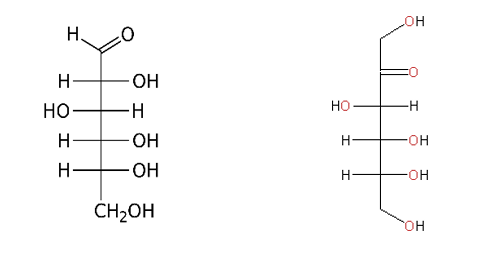
Figure 4 (viii). Formes ouvertes du glucose (à gauche) et du fructose (à droite)
Le glucose peut s'additionner aux DAF en les glycosylant, ce qui donne des glucosyl-DAF (plusieurs, selon le groupe OH auquel il s'attache). Il peut aussi se polymériser en oligosaccharides. Sous la dénomination polydextrose, ces polymères (fig. 5) sont des additifs alimentaires autorisés utilisés comme « agents de charge » sous la dénomination de E1200. Un agent de charge est un composé qui n'est pas digestible et augmente la quantité de produit sans augmenter la valeur énergétique (ici, 1 kcal/g).
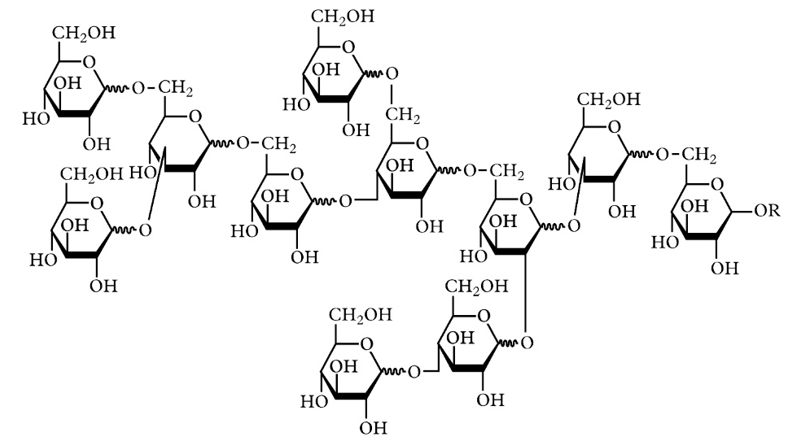
Figure 5. Exemple de polydextrose (agent de charges)
Source Heli Putaala
Authentification des caramels
Le caramel dit « aromatique » est un ingrédient largement utilisé pour l’aromatisation des desserts lactés, et le caramel « colorant » est un additif de nombreuses boissons, eaux de vie, aliments pour animaux ou encore de produits pharmaceutiques. Ces deux types de caramels sont définis depuis 1988 par la norme Afnor NF V00-100 (ix), comme devant provenir exclusivement du traitement thermique ménagé de sucres alimentaires en présence de catalyseurs définis (jus de citron, vinaigre, acide citrique...). Pour contrôler ces caramels, on peut rechercher l'agent odorant 5-(hydroxyméthyl)-2-furfuraldéhyde (fig. 2) , mais comme ce produit est commercial et bon marché, il pourrait donc être volontairement ajouté, ce qui rend sa seule recherche peu sûre. La recherche des DAFs est un moyen plus efficace de contrôle de l'authenticité des caramels commerciaux.
En cette période de consommation de friandises, il est important de savoir ce que l'on mange !
Nicole Moreau et l’équipe Question du mois
(i) Dictionnaire historique de la langue française, édition Le Robert
(ii) par exemple, dans le célèbre Carambar, on peut trouver : mono- et diglycérides d'acides gras – sirop de glucose – lait écrémé concentré sucré – sucre – huile de coprah hydrogénée – cacao maigre en poudre – sel – arôme artificiel – gélatine – cannelle, ou autres suivant le type de carambar.
(iii) H. This « A propos de caramel .
(iv) On trouve parfois le nom de sucrose, qui ne doit pas être utilisé en français, car c'est un " faux ami ", c'est le mot anglais désignant le saccharose. Le nom du saccharose dans la nomenclature est le α-D-glucopyranosyl-(1-2)-β-D-fructofuranoside.
(v) Les sucres simples sont des monosaccharides ou monoses. On parle ensuite de di-, tri-saccharides, etc.
(vi) saccharose, Don A. Carlson, Wikimedia Commons, licence CC BY-SA 3.0
glucose ou α-D-glucopyranose, Wikimedia Commons, domaine public
fructose ou β-D-fructofuranose, Wikimedia Commons, domaine public
(vii) 5-(hydroxyméthyl)-2-furfuraldéhyde , Wikimedia Commons, domaine public
(viii) glucose Christopher King, travail personnel, Wikimedia Commons, licence CC BY-SA 3.0
fructose , Wikimedia Commons, licence GPL
(ix) Afnor NF V00-100
Pour en savoir plus
[1] Péligot E., Ann. Chim. Phys., 2nd Ser. (1838) 67, p. 113
[2] Cottier L., Descotes G., Neyret C., Nigay H., Ind. Aliment. Agric. (1989) 106, p. 567
[3] Ledl F., Schleicher E., Angew. Chem., Int. Ed. Engl. (1990) 29, p. 565
[4] Les molécules de la caramélisation : structure et méthodologies de détection et d'évaluation, Defaye J., Garcia Fernandez J.M., Ratsimba V., L'Actualité chimique (novembre 2000) p. 26-27
[5] Et pour sourire à propos du caramel : « Caramel » - produit du jour- Société Chimique de France (SCF)
Crédit illustration : --Where next Columbus? (talk) Wikimedia Commons, licence CC BY-SA 3.0











